Guo, J., Feng, K., Wu, W., Ruan, Y., Liu, H., Han, X., ... & Sun, X. (2021). Smart 131I labeled self‐illuminating photosensitizers for deep tumor imaging guided therapy. Angewandte Chemie.1
1. 개요
2. 결과
3. 한계
1. 개요
⑴ PDT(photodynamic therapy)
① 원리 : 빛을 받으면 PS(photosensitizer)가 활성산소(reactive oxygen species, ROS)를 방출하는 것을 이용
② 장점 : spatial selectivity와 temporal selectivity가 높아 각광받고 있음
③ 경우 1. 가시광선, 자외선 : 조직 투과도가 떨어짐
④ 경우 2. 적외선, X선 : 피부 부근의 손상이 우려
⑤ 경우 3. 외부 광원을 필요로 하지 않는 경우
⑥ 3-1. bioluminescence 또는 chemiluminescence : 효소나 H2O2 수치에 영향을 많이 받아 제어하기 어려움
⑦ 3-2. 체렌코프 방사(Cerenkov radiation, CR)를 이용하는 경우
○ PS와 radiopharmaceutical이 결합하지 않은 경우 : 효율성이 떨어짐
○ PS와 radiopharmaceutical이 결합한 경우 : phototoxicity와 safety issue가 있음
⑵ 131I-sPS 시스템의 구성
① PPa(pyropheophorbide-a) : PS
○ 임상적으로 이용 가능한 PS
○ 400 nm에서 흡광도 피크를 가져 체렌코프 방사에 반응할 수 있음
② DPA(diisopropylamino group) : pH-sensitive group
③ 131I-labeled tyrosine group : CR donor
④ PEG(polyethylene glycol) : 친수성이 강하기 때문에 소수성이 강한 나머지 부분과 함게 self-assemble 반응을 수행
⑶ 131I-sPS 시스템의 원리

Figure. 1. 131I-sPS 시스템의 원리
① 1st. 합성 당시 소수성 상호작용에 의해 self-assemble 반응을 수행
② 2nd. 131I는 PEG 등에 의해 가려져 ACQ(aggregation-caused quenchinig) : 정상 조직에 대한 phototoxicity가 낮음
③ 3rd. 131I-sPS가 세포 내로 쌓인 뒤 낮은 pH 환경에 노출되면 DPA가 protonation됨
④ 4th. disassembly : self-assemble 반응이 풀림
⑤ 5th. 친수성 바깥 부분에 노출되었던 131I에 의한 체렌코프 방사는 인접한 원자단에 의해 더 긴 파장으로 전환
○ 이를 CRET(Cerenkov radiation energy transfer)라고 함
⑥ 6th. PS는 CRET를 흡수하고 ROS를 생성
2. 결과
⑴ 일반 특성 평가
① TEM 결과
○ pH 7.4인 PBS에서 100.00 ± 5.32 nm
○ pH 5.4에서 disassembly가 잘 일어남을 보여줌
② DLS 결과
○ hydrodynamic size를 본 결과 시간에 따라 안정하고 FBS에서도 안정하나 pH 6.5에도 disassembly
○ 계면활성제인 SDS를 첨가하자 hydrodynamic size가 크게 감소함 : 소수성 상호작용이 주된 메커니즘임을 밝힘
③ 흡광도 및 형광
○ 흡광도 : pH-independent. sPS의 화학적 구조가 보존됨을 보여줌
○ 660-700 nm 형광 : pH 낮아짐 → disassembly → PS가 노출됨
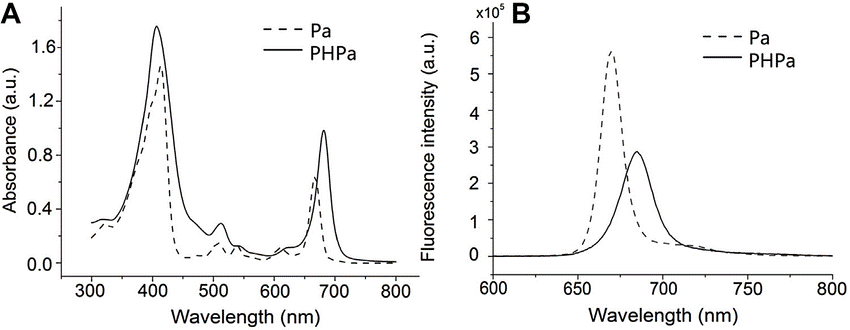
Figure. 2. (참고) PPa의 흡광도와 형광2
④ SOSG(singlet oxygen sensor green)
○ ROS가 생성되면 510-560 nm 형광이 나타나는 키트
○ 405 nm 레이저 유무에 따른 510-560 nm 형광 : pH 낮아짐 → PS가 노출됨 → 레이저에 의해 ROS가 나타남
⑵ radiolabeling 특성 평가
① radio-HPLC
○ radiochemical yield : 75.27 ± 2.46 %
○ radiochemical purity : 92.30 %
○ 다양한 용매에서 radiostability가 뛰어남
② 형태 및 광학적 특성
○ radiolabeling은 형태나 광학적 특성을 변화시키지 않음
③ radioisotope가 생성한 체렌코프 방사에 의한 SOSG 형광
○ pH가 낮아질수록 형광 세기가 세짐
⑵ in vitro 실험
① in vitro 형광
○ pH 6.5 배지에서 4T1 세포를 키우고 pH 7.4 배지에서 L02 세포를 키운 뒤 형광 세기를 측정
○ pH 6.5 배지에서 키운 4T1 세포 배양용기에서 더 큰 형광이 관찰됨
② MTT assay : 405 nm 레이저를 쏨
○ sPS : IC50는 4T1 기준 1.0 mg/mL, L02 기준 8.0 mg/mL
○ "always-on" PS (DPA가 없음) : IC50는 4T1 및 L02 모두에서 1.0 mg/mL로 관찰
○ "always-off" PS (DPA를 교체) : 세포 독성이 없음
③ radioiodine labeling 후 퍼포먼스
○ 131I의 dose를 증가시키자 Na131I, sPS와 달리 131I-sPS의 세포 독성이 증가함
○ DCFH-DA(2,7-dichlorofluorescin diacetate) 반응 결과 131I-sPS의 ROS 생성이 확인됨
○ γ-H2AX assay 결과 ROS에 의한 DNA 이중나선 결합의 파괴가 131I-sPS에서만 관찰됨
○ CR이 레이저보다 약하지만 비슷한 세포 독성을 보인다는 사실은 주목할 만함 (∵ CR은 레이저와 달리 지속적)
○ 131I-sPS의 cell uptake 효율은 4T1에서가 L02 세포에서보다 큼
○ 이는 4T1 세포에서 131I-sPS의 protonation이 음하전을 띠는 세포막과 정전기적 결합을 했기 때문으로 여겨짐
○ 4T1 pH 6.5 > 4T1 pH 7.4 > ··· > L02 pH 7.4 순으로 세포 독성이 강함
○ 위 경향성은 Calcein-AM assay 및 PI(propidium iodide) assay 결과를 통해 뒷받침됨
○ DCF assay 결과 위 경향성은 ROS 때문인 것으로 여겨짐
○ 131I-off-PS는 거의 세포 독성을 보이지 않음
○ 131I-on-PS는 4T1과 L02 세포 모두에 세포 독성을 보임
⑶ subcutaneous in vivo 실험
① biodistribution
○ 131I-sPS로부터 떨어져 나온 131I가 갑상선으로 가지 않아 뛰어난 radiostability를 엿볼 수 있음
② tumor volume, body weight 및 survival rate
○ 131I-sPS는 131I-off-PS, Na131I, sPS에 비해 우월한 in vivo 퍼포먼스를 보여줌
○ 그러면서 body weight로 보건데 마우스에 큰 악영향을 주지 않음
③ H&E 염색
○ 131I-sPS에 의한 염증이나 조직 손상이 관찰되지 않음
⑷ orthotopic in vivo 실험 : deep tumor에 대한 치료 효과를 확인하기 위함
① 18F-FDG PET
○ VX2 tumor implant가 제대로 형성됨을 보여줌
② SPECT
○ 131I-sPS의 종양 내 섭취를 확인함
③ γ-counting
○ 131I-sPS의 종양 내 섭취를 확인함
④ 18F-FDG PET에서 SUVmax 값의 조사
○ 131I-sPS의 종양 억제 효과를 보여주듯 SUVmax가 혼자만 작음
⑤ H&E 염색, Ki-67 면역 염색, TUNEL assay
○ 131I-sPS의 뛰어난 효과를 보여줌
3. 한계
⑴ 131I-sPS, 131I-off-PS, Na131I, sPS를 넣었을 때 biodistribution의 차이를 보지 않음
① pH-sensitivity가 tumor uptake에 영향을 줄 수도 있기 때문에 보았으면 좋았을 부분
⑵ orthotopic model을 왜 만들었는지에 대한 이유 소명이 부족함
⑶ 면역계 분석이 없음
⑷ cell uptake 전에 disassembly를 했을 가능성에 대한 고려가 필요함
입력 : 2021.09.15 22:51



최근댓글