1-1강. 루이스 구조식
추천글 : 【유기화학】 1강. 유기화학의 기초
1. 루이스 구조식 그리는 법 [본문]
2. 루이스 구조식 규칙성 [본문]
3. 까다로운 루이스 구조 [본문]
1. 루이스 구조식 그리는 법 [목차]
⑴ 1st. 각 원자의 나열순서를 결정한 뒤 모든 원자의 원자가 전자를 표시

Figure. 1. 루이스 구조식 1단계
CNO-에서 과잉 전자 1개는 어떤 원자에 할당해도 무방
⑵ 2nd. 임의로 이들 원자들을 연결

Figure. 2. 루이스 구조식 2단계
⑶ 3rd. 적절히 전자를 이동시켜 옥텟 규칙을 만족하도록 함

Figure. 3. 루이스 구조식 3단계
① 전자의 이동은 공명의 규칙에 제한될 필요가 없음
② 옥텟 규칙 반례 : 라디칼이 존재할 수 있음
③ 2주기 원자의 경우 절대 최외각전자가 8개를 초과해서는 안 됨
⑷ 4th. 여러 가지 구조가 가능하다면 형식전하를 고려

Figure. 4. 루이스 구조식 4단계
2. 루이스 구조식 규칙성 : 항상 들어맞는 것은 아님을 주의 [목차]
⑴ 다이보레인(diborane) 등을 제외하고는 H는 항상 말단원자(terminal atom)
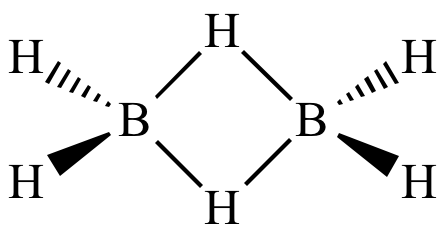
Figure. 5. 다이보레인의 구조
⑵ 중심원자(central atom)는 이온화에너지가 가장 작은 원자로 선택
⑶ 중심원자 주위로 원자들이 대칭적으로 배치
① 예. SO2는 SOO가 아니고 OSO와 같이 배열
② 반례. N2O는 NON이 아니고 NNO와 같이 배열
⑷ 간단한 원자의 경우 중심원자는 첫 번째로 기입됨
① 예. OF2는 OFF가 아니고 FOF와 같이 배열
② 반례. 산의 경우; H2S는 HSH가 HHS가 아니고 HSH와 같이 배열
⑸ 옥소산(oxoacid)의 경우 H는 O와 붙어 있음
① 예. H2SO4 = (HO)2SO2
3. 까다로운 루이스 구조 [목차]
⑴ CNO-

Figure. 6. fulminate의 구조
⑵ N2O

Figure. 7. nitrous oxide
⑶ NO2 : 산소에 라디칼이 있는 구조도 가능함을 주의

Figure. 8. nitrogen oxide
⑷ NO2+

Figure. 9. nitronium ion
⑸ NO2-

Figure. 10. nitrogen oxide anion
⑹ NO3

Figure. 11. nitrogen trioxide
⑼ NO3- : HNO3 또는 HONO2의 구조

Figure. 12. nitrate ion
⑽ O3

Figure. 13. ozone
⑾ SO2
① 옥텟 규칙의 확장이 적용
② 실제 구조는 S에 +2의 형식전하가 있는 구조로 sp2 혼성

Figure. 14. sulfur dioxide
⑿ SO3
① 옥텟 규칙의 확장이 적용
② 실제 구조는 S에 +3의 형식전하가 있는 구조로 sp2 혼성

Figure. 15. sulfur trioxide
⒀ SO42-

Figure. 16. sulfate ion
입력 : 2019.03.23 13:34
'▶ 자연과학 > ▷ 유기화학' 카테고리의 다른 글
| 【유기화학】 10강. 콘쥬게이션 화학 (9) | 2019.01.04 |
|---|---|
| 【유기화학】 9강. 라디칼 반응 (11) | 2019.01.04 |
| 【유기화학】 8강. 알켄 및 알카인 (59) | 2018.12.27 |
| 【유기화학】 7강. 할로젠화 알킬 (17) | 2018.12.27 |
| 【유기화학】 5강. 유기반응 개요 (4) | 2018.12.27 |




최근댓글