2017 MEET/DEET 화학 (예비검사)
추천글 : 【화학】 MEET/DEET 화학 풀이
1. 바닥 상태의 126C 원자에 대한 설명으로 옳지 않은 것은?
⑴ 문제

⑵ 풀이 : ②
①, ② 중성자 개수 6개 + 양성자 개수 6개 = 핵자 12개
③, ④, ⑤ 전자 배치는 1s22s22p2이므로 홀전자가 2p 오비탈에 총 2개 있음
2. 그림은 질소(N)의 원자 오비탈로부터 만들어진 N2 분자 궤도함수의 에너지 준위 일부를 나타낸 것이다. 분자 궤도함수 이론을 근거로 바닥 상태의 세 화학종 N2, N2+, N2-에 대하여 설명한 것으로 옳지 않은 것은? (단, 원자, 분자, 이온에 전자가 제거되거나 추가되어도 궤도함수의 에너지는 변하지 않는다고 가정한다.)
⑴ 문제


⑵ 풀이 : ④
① N2는 그림에 표시된 대로 홀전자가 없으므로 반자기성
② N2+ (σ2s2σ*2s2π2p4σ2p1)의 결합 차수는 5 / 2 = 2.5
③ N2-와 N2의 결합 차수는 각각 2.5, 3이므로 결합 차수가 작은 N2-가 더 결합 길이가 긺
④ N2-와 N2의 HOMO는 각각 π*2p, σ2p이므로 HOMO의 에너지 수준이 더 높은 N2-가 일차 이온화 에너지가 더 작음
⑤ N2-는 π*2p에도 전자가 차 있지만 N2+는 그렇지 않으므로 맞는 설명
3. N2O 분자의 원자 배열 순서는 NNO이다. 가장 타당한 루이스 구조를 근거로, 원자가 껍질 전자쌍 반발 이론과 원자가 결합 이론을 적용하여 이 분자에 대해 설명한 것으로 옳지 않은 것은?
⑴ 문제

⑵ 풀이 : ③
① 가장 타당한 루이스 구조를 그리면 공명 구조로 인해 N, N, O가 일직선에 놓이게 됨
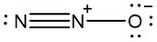
② N-N 결합에 2개의 π 결합이 있음
③ 산소의 형식 전하는 -1
④ 2주기 원자는 무조건 팔전자 규칙을 만족해야 함 (∵ d 오비탈이 없으므로)
⑤ 중심의 질소는 sp 혼성 오비탈 및 2개의 π 오비탈을 가짐
4. N3-, F-, Na+, Mg2+은 바닥 상태에서 동일한 전자 배치를 갖는다. 이들 이온에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제

⑵ 풀이 : ③
ㄱ. Ne과 전자 배치가 동일함
ㄴ. 전자 배치가 동일할 때 원자 번호가 클수록 이온 반지름이 작아짐
ㄷ. 전자 배치가 동일할 때 원자 번호가 클수록 이온 반지름이 작아짐
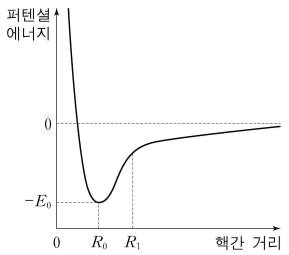
5. 그림은 25 ℃, 1 atm에서 동핵 이원자 분자의 핵간 거리에 따른 퍼텐셜 에너지를 나타낸 것이다. (R0은 분자의 퍼텐셜 에너지가 최소일 때의 핵간 거리이다.) 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, NA는 아보가드로 수이다.)
⑴ 문제

⑵ 풀이 : ②
ㄱ. 동핵 이원자 분자의 표준 생성 엔탈피는 0으로 정의
ㄴ. F는 2주기 원소이고, Cl은 3주기 원소이므로 F2가 Cl2보다 분자 간 거리가 작음
ㄷ. 핵간 거리 R1가 됐다는 것은 단순히 각 원자들이 멀어진 것으로, 대칭성은 유지되어 분자의 쌍극자 모멘트는 0
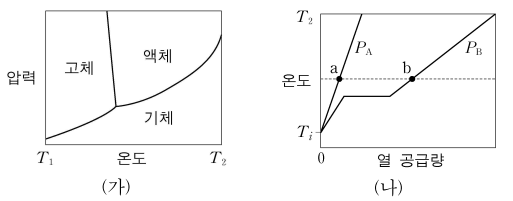
6. 그림 ㈎는 물질 X의 상그림을, 그림 ㈏는 서로 다른 압력 PA와 PB에서 일정량의 X에 대해 얻어진 가열 곡선을 나타낸 것이다. 이에 대한 설명으로 옳지 않은 것은? (단, Ti, PA, PB는 그림 ㈎의 온도와 압력 범위 내에 있으며 X의 상태에 따른 비열의 크기는 액체 > 고체 > 기체이다.)
⑴ 문제

⑵ 풀이 : ④
① PB에서의 가열 곡선에서 비열이 작았다가 상 변화 이후 비열이 커지므로, 고체 → 액체가 되는 과정이므로 Ti < Tc
② PA에서의 가열 곡선의 비열이 PB에서의 어떤 상보다 작으므로 기체이고, 이로 인해 PA는 PB임을 알 수 있음
③ PB에서 녹는점은 수평으로 그래프가 나타나는 구간에서의 온도
④ 기체상이 액체상보다 상태수(≒ 경우의 수)가 훨씬 크므로 엔트로피는 a가 b보다 큼
⑤ 그림 ㈎를 보면 X의 녹는점은 압력이 높을수록 낮음 (e.g., 물)
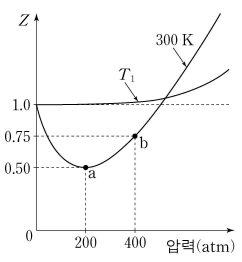
7. 그림은 온도가 각각 300 K와 T1일 때 어떤 기체 1몰에 대하여 압력에 따른 압축 인자(Z = PV / RT)를 나타낸 것이다. 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제

⑵ 풀이 : ⑤
ㄱ, ㄴ. 온도가 높을수록 이상 기체에 가까운 거동, 즉 Z = 1에 가까워짐
ㄷ. Va : Vb = ZaR × 300 / Pa : ZbR × 300 / Pb = 0.50 / 200 : 0.75 / 400 = 4 : 3
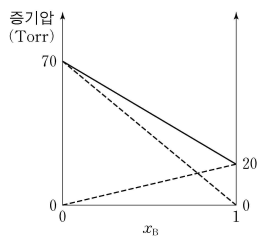
8. 그림은 액체 A와 액체 B의 혼합 용액에서 B의 몰분율(xB)에 따른 각 성분의 증기압(---)과 전체 증기압(―)을 나타낸 것이다. 이에 대한 설명으로 옳지 않은 것은?
⑴ 문제

⑵ 풀이 : ④
① 혼합 용액의 증기압이 직선의 형태로 나타나므로 라울의 법칙을 만족하는 이상 용액
② 순수한 액체 B의 증기압은 xB = 1에서의 증기압인 20 Torr
③ 순수한 액체 A의 증기압은 70 Torr이므로 증기압과 경향성이 반대인 분자 사이의 인력은 B가 A보다 큼
④ xB = 0.6에서의 전체 증기압은 20 × 0.6 + 70 × 0.4 = 12 + 28 = 40 Torr
⑤ xB = 0.4일 때 증기에서 B의 몰분율은 0.4 × 20 / (0.4 × 20 + 0.6 × 70) = 8 / 50 = 0.16
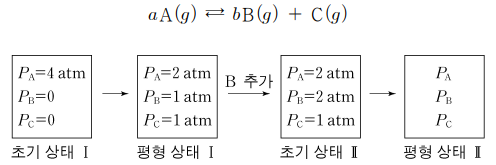
9. 다음은 기체 화합물 A가 B와 C로 분해되는 반응식이고, 그림은 반응물과 생성물의 시간에 따른 부분 압력의 변화를 나타낸 것이다. 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 반응 과정에서 온도와 부피는 일정하다.)
⑴ 문제

⑵ 풀이 : ②
ㄱ. 온도와 부피가 일정할 때 압력을 몰수처럼 생각할 수 있음. a : b : c = 4 atm - 2 atm : 1 atm : 1 atm = 2 : 1 : 1
ㄴ. Kp = 1b × 1 / 2a = 1 × 1 / 22 = 1/4
ㄷ. 계산 과정
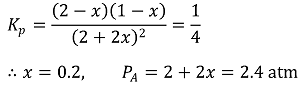
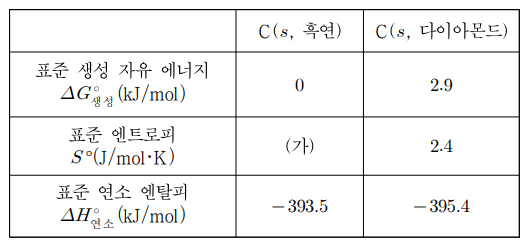
10. 표는 25 ℃에서 흑연과 다이아몬드의 열화학 자료를 나타낸 것이다. 위의 자료를 근거로 옳게 설명한 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제

⑵ 풀이 : ③
ㄱ. C(s, 흑연) + O2 (g) → CO2 (g)의 반응 엔탈피가 -393.5 kJ/mol이고, C(s, 흑연) 및 O2 (g)의 표준 생성 엔탈피는 0이므로 CO2 (g)의 표준 생성 엔탈피가 -393.5 kJ/mol임을 알 수 있음
ㄴ. C(s, 흑연) + O2 (g) → CO2 (g)의 반응 엔탈피가 -395.4 kJ/mol이라는 점으로부터, C(s, 흑연)의 표준 생성 엔탈피가 1.9 kJ/mol임을 알 수 있음
ㄷ. 우선 표준 엔트로피(0 K, 고체 격자 기준)와 표준 반응 엔트로피가 다름을 이해 (ref)
0 = 0 - 298 × ΔSºC(s, 흑연)
2.9k = 1.9k - 298 × ΔSºC(s, 다이아몬드)
로부터 ΔSºC(s, 다이아몬드) > ΔSºC(s, 흑연)임을 알 수 있음. Sm, C(s, 다이아몬드)가 2.4 J/mol·K로 주어져 있으므로 Sm, C(s, 흑연)은 그보다는 작아야 함
11. 다음은 LiBr과 KBr의 용해 엔탈피를 측정하는 실험이다. 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, LiBr 수용액과 KBr 수용액의 비열은 4.2 J/g·℃이다.)
⑴ 문제


⑵ 풀이 : ③
ㄱ. LiBr의 용해 엔탈피 계산 과정
○ LiBr 수용액의 무게 : 108.7 g
○ LiBr 용해 반응으로부터 방출된 열 : 108.7 g × 4.2 J/g·℃ × 10.7 ℃ = 108.7 × 4.2 × 10.7 J
○ LiBr의 몰 용해 엔탈피 : -108.7 × 4.2 × 10.7 / 0.10 J/mol
ㄴ. KBr의 용해 결과 수용액의 온도가 감소했으므로 KBr의 용해는 흡열 반응
ㄷ. KBr의 용해 엔트로피 > 0이지만 (∵ 분자 자유도 증가), ΔG = ΔH - TΔS < 0이므로 자발적 반응이 일어나게 됨
12. 반응물 A가 생성물 P로 변환되는 반응에 대하여, 그림 ㈎와 ㈏는 100 K와 200 K에서 각각 [A]와 1 / [A]을 시간에 따라 나타낸 것이다. 이 반응에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 기체 상수 R는 8.31 J/mol·K이다.)
⑴ 문제
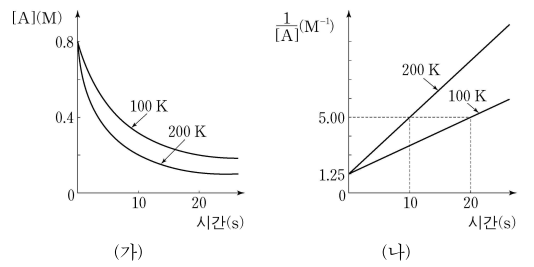

⑵ 풀이 : ⑤
ㄱ, ㄴ. 2차 반응 : 1 / [A] = 1 / [A]0 + kt
ㄷ. 계산 과정
○ 아레니우스 식 : k = A exp (-Ea / RT) ⇔ ln k = ln A - Ea / RT
○ k200K = 0.375 M-1s-1
○ k100K = k200K / 2
○ ln k200K / k100K = -(Ea / R) × (1 / 200 - 1 / 100)
○ ∴ Ea = ln 2 × 8.31 × 200 J/mol
13. 다음은 일산화 질소(NO)의 분해 과정에 대해 제안된 반응 메커니즘이며, 사전평형(pre-equilibrium) 근사법을 적용한 전체 반응의 속도 상수는 k이다. 이 반응에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제
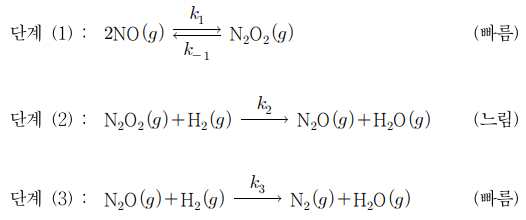

⑵ 풀이 : ③
ㄱ. 최종 반응식 : 2NO + 2H2 → N2 + 2H2O
ㄴ. 반응 속도식 : 사전평형 근사법
○ k1[NO]2 = k-1[N2O2]
○ ∴ v = k2[N2O2][H2] = (k2k1/k-1) × [NO]2[H2] = k[NO]2[H2]
ㄷ. H2의 농도를 2배로 하면 반응 속도는 2배가 됨
14. 삼양성자산 H3A는 다음과 같이 해리한다. 1.0 M H3A 수용액의 평형에서의 H3A, H2A-, HA2-, A3-, H+의 농도를 구한 것으로 옳지 않은 것은?
⑴ 문제
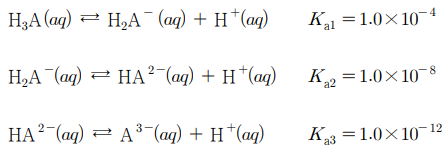
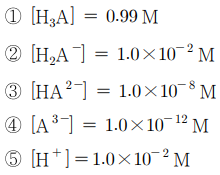
⑵ 풀이 : ④
①, ②, ⑤ Ka1 = 10-4 = [H2A-][H+] / [H3A] = x2 / (1-x). ∴ x = [H2A-] = [H+] = 1 - [H3A] = 0.01 M
③ Ka2 = 10-8 = [HA2-][H+] / [H2A-] = y × 0.01 / 0.01 = y. ∴ y = [HA-] = 10-8 M
④ Ka3 = 10-12 = [A3-][H+] / [HA2-] = z × 0.01 / 10-8 = z × 106. ∴ z = [A3-] = 10-18 M.
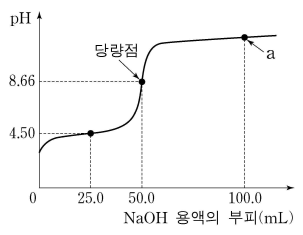
15. 그림은 25 ℃에서 약산 HA (산 해리 상수 Ka) 수용액 100.0 mL를 0.20 M NaOH 표준 용액으로 적정할 때의 이론적인 적정 곡선을 나타낸 것이다. 사용한 지시약 HIn (산 해리 상수 KIn)의 pKIn는 8.40이다. 이에 대한 설명으로 옳지 않은 것은? (단, 25 ℃에서 물의 자체 이온화 상수 Kw는 1.0 × 10-14이다.)
⑴ 문제

⑵ 풀이 : ⑤
① pKa + pKb = pKw = 14
② [HA] × 100 mL = 0.20 M NaOH × 50 mL ⇔ [HA] = 0.10 M
③ pKa = 반당량점에서의 pH = 4.50
④ 당량점에서의 pH = 8.66 = pKIn + log([In-] / [HIn]) ⇔ [In-] / [HIn] > 1
⑤ a에서의 [OH-] = 50 mL × 0.20 M NaOH / 200 mL = 0.05 M. ∴ pH = 14 - pOH = 12.7
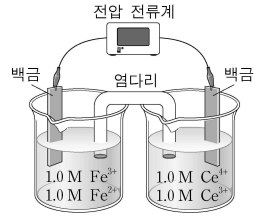
16. 그림은 백금 전극을 사용한 두 반쪽 전지를 염다리로 연결한 갈바니 전지를 나타낸 것이다. 왼쪽 비커에는 Fe3+와 Fe2+의 농도가 각각 1.0 M인 수용액 100 mL를 넣었다. 다음은 각 반쪽 전지의 반응식과 25 ℃에서의 표준 환원 전위(Eº)이다.
Ce4+ (aq) + e- ⇄ Ce3+ (aq), Eº = 1.70 V
Fe3+ (aq) + e- ⇄ Fe2+ (aq), Eº = 0.77 V
25 ℃에서 이 전지에 대한 설명으로 옳지 않은 것은?
⑴ 문제

⑵ 풀이 : ②
① 전지의 초기 기전력은 1.70 - 0.77 = 0.93 V
② 네른스트 공식에서 E = Eº - (0.0592 / 2) log Q, Q = ([Ce3+][Fe3+]) / ([Ce4+][Fe2+])이므로, 이온의 농도를 묽힌다 하여 이온들의 조성비가 바뀌는 것은 아니므로 전지의 기전력은 바뀌지 않음
③ 전자는 Fe2+/Fe3+ 반쪽 전지에서 나와 Ce3+/Ce4+ 반쪽 전지로 이동 (∵ Ce4+의 환원전위가 더 높으므로)
④ 평형상수에 대한 표현을 묻는 것
⑤ Ce3+/Ce4+에서 침전하거나 용출되는 이온은 없으므로 백금 전극 진량은 변화하지 않음
17. 다음은 금(Au)이 HNO3와 HCl의 혼합 수용액에서 용해되는 반응이다. 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제
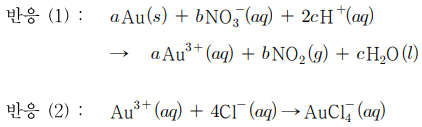

⑵ 풀이 : ①
○ 산화 반응 ⒜ : Au → Au3+ (Au의 산화수 +3)
○ 환원 반응 ⒝ : NO3- → NO2 (N의 산화수 -1)
○ ⒜가 1번 일어날 동안 ⒝가 3번 일어나야 함
○ 산소 개수 차이는 H2O, H+로 맞추어야 함
○ a = 1이라고 가정
○ Au + 3NO3- + 6H+ → Au3+ + 3NO2 + 3H2O
○ 전하 균형을 보면서 최종식을 검토
○ 따라서 3a = b가 성립
ㄴ. NO3-은 환원하므로, 다른 물질을 산화시키는 산화제로 작용
ㄷ. 반응 ⑵는 산화환원반응이 아니라 산·염기 반응이므로 산화, 환원하는 화학종이 없음
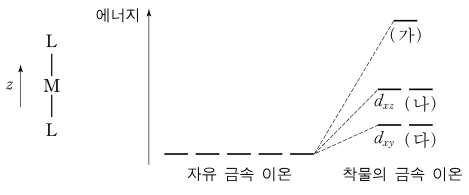
18. 그림은 직선형 구조를 갖는 ML2 착물의 중심 금속 이온 M의 d 오비탈 에너지 갈라짐을 결정장 이론을 적용하여 나타낸 것이다. ㈎ ~ ㈐에 해당하는 오비탈을 옳게 짝을 지은 것은?
⑴ 문제
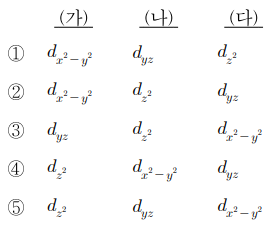
⑵ 풀이 : ⑤
○ 필수 암기 사항
○ 팁 1. dxz와 dyz는 항상 붙어 다님
○ 팁 2. dz2, dx2-y2이 헷갈리는 상황에서 dxy와 dx2-y2이 같이 있는 게 더 자연스러움 (cf. x, y로만 구성)
19. 그림은 K2PtCl6로부터 두 개의 백금 착물 cis-Pt(NH3)2Cl2와 Pt(en)Cl2를 각각 합성하는 경로를 나타낸 것이다. (en은 H2NCH2CH2NH2이다.) 이에 대한 설명으로 옳은 것은?
⑴ 문제
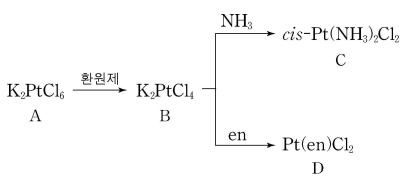

⑵ 풀이 : ①
① 산화수 개념
② B에서 Pt의 배위수는 4 : Cl-가 4배위로 결합
③ C는 cis 구조이므로 전기음성도가 큰 질소쪽으로 전자가 쏠림 → 쌍극자 모멘트(방향 : (+)극 → (-))가 0이 아님
④ 사각형 구조를 가지는 D는 기하 이성질체를 가지지 않음
⑤ C, D에서 Pt의 산화수가 모두 +2이지만, 3d 오비탈보다 먼저 4s 오비탈이 해리되므로 모두 [Xe]4f145d8의 전자배치
20. 다음은 주어진 온도와 압력에서 기체 시료의 부피와 질량을 측정하여 분자량을 결정하는 실험이다. 이에 대한 설명으로 옳지 않은 것은? (단, 기체 상수 R는 0.0821 atm·L/mol·K이다.)
⑴ 문제


⑵ 풀이 : ⑤
① 알루미늄 포일로 씌우고 중앙 부분에 바늘로 작은 구멍을 뚫는 것은 플라스크 내부 압력을 대기압으로 맞추려는 것
② 물기를 완전히 닦지 않으면 물기의 무게마저 시료의 무게로 보기 때문
③ 액체 시료 중 일부는 대기로 날았으며, 일부는 플라스크 안을 채우고 있고, 다른 일부는 아직 증발하지 않은 채 과정 ㈓에서 플라스크 내에 여전히 응축돼 있음
④ 시료 기체의 무게는 0.326 g (∵ 양압이므로 플라스크 내부에 공기 분자는 없다고 가정)
⑤ PV = nRT ⇔ μ = mRT / PV이므로 μ = 0.326 × 0.0821 × (273 + 90) / 0.993 / 0.3045 g/mol
입력 : 2023.07.22 16:10
'▶ 자연과학 > ▷ MEET∙DEET∙PEET 풀이' 카테고리의 다른 글
| 【유기화학】 2020 PEET 유기화학 (4) | 2021.07.23 |
|---|---|
| 【유기화학】 2021 PEET 유기화학 (4) | 2021.07.15 |
| 【유기화학】 2021 MEET/DEET 유기화학 (10) | 2020.08.26 |
| 【화학】 2016 MEET/DEET 화학 (6) | 2020.06.30 |
| 【유기화학】 2004 MEET/DEET 유기화학 (0) | 2020.03.06 |




최근댓글