2021 PEET 유기화학
추천글 : 【유기화학】 PEET 유기화학 풀이
1. 다음은 라디칼 반응의 출발 물질 A와 생성물 B의 구조를 나타낸 것이다. 이에 대한 설명으로 옳은 것은?
⑴ 문제

⑵ 풀이 : ③
○ 전파단계 메커니즘은 다음과 같음

① 5개임
② A와 B의 불포화도는 7임 (∵ 고리 및 이중결합 개수)
③ B는 trans-decalin을 부분 구조로 포함함

④ B의 카이랄 중심(chiral center)은 모두 7개임 (∵ 카이랄 중심은 원칙상 서로 다른 치환기를 가짐 (ref)
⑤ (R) 배향 : 아래 그림에서 숫자는 CIP 우선순위를 나타냄. RS 판별법과 벡터의 외적 참고
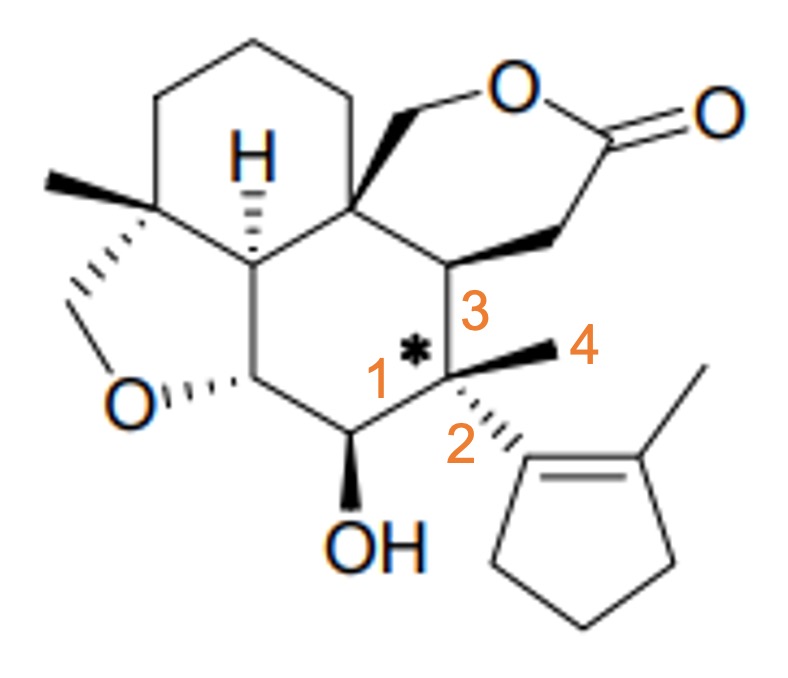
2. 화합물의 구조 또는 물리화학적 성질에 대한 비교가 옳은 것은?
⑴ 문제
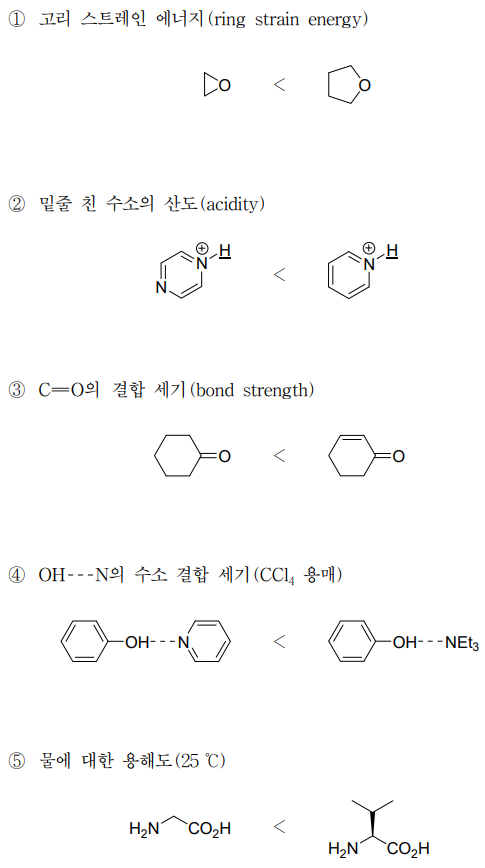
⑵ 풀이 : ④
① sp3의 결합각은 109.5°이므로 이것과 차이가 큰 삼각형 형태가 고리 스트레인이 큼
② 좌측 형태에서 수소가 붙어 있지 않은 질소 원자는 전자 당김 유발효과를 일으켜 산도를 높임
③ 좌측 형태는 이중 결합에 가깝고 우측 형태는 공명으로 인해 단일결합과 이중결합의 사이
④ 좌측의 pyridine의 질소의 비공유전자쌍은 공명에 참가하여 수소 결합에 참여할 수 없음
⑤ 우측 형태는 탄화수소 체인이 붙어있어서 lipid-like 하기 때문에 소수성이 증가함
3. 각 반응에서 두 화합물의 반응 속도 비교가 옳은 것은?
⑴ 문제
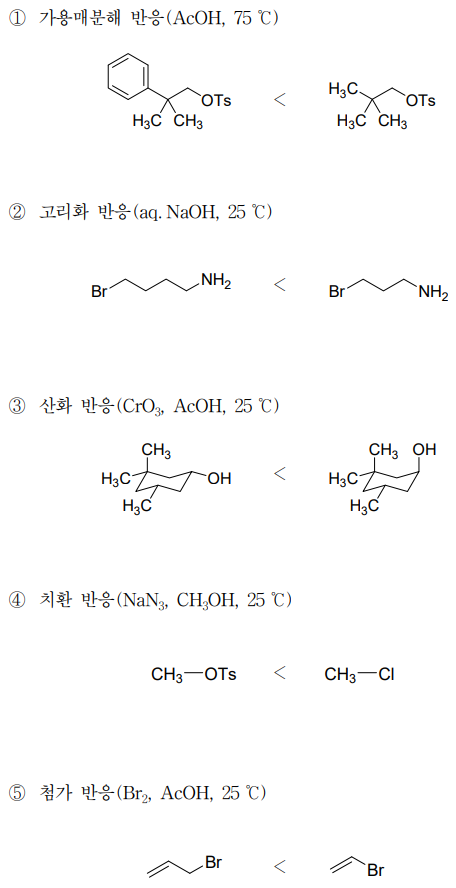
⑵ 풀이 : ③
① 이탈기가 이탈한 뒤 1,2-methyl shift가 일어나면 3차 carbocation이 발생 → 벤젠기의 안정화효과가 크게 관여
② 아민기가 친핵체 공격을 하여 Br기가 이탈하는 반응. 오각형이 형성되는 좌측이 사각형이 형성되는 우측보다 안정
③ CrO3 반응 메커니즘
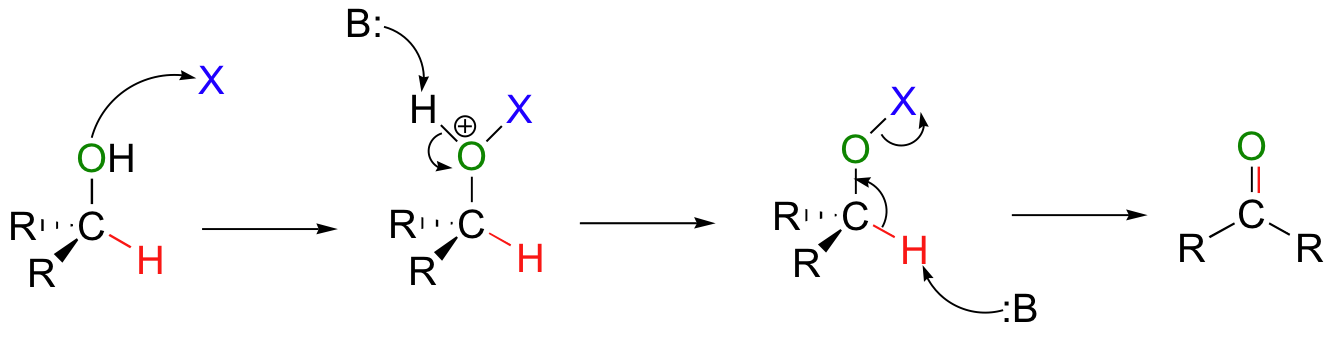
○ 전자 반발이 적게 CrO3가 접근해야 하므로 -OH기가 axial일 때 산화반응이 일어남
○ 좌측 형태는 ring-flip이 일어나면 -OH기가 axial이 되고 CH3-OH 1,3-diaxial interaction이 두 개가 존재함
○ 우측 형태는 -OH기가 axial이고 CH3-OH 1,3-diaxial interaction이 한 개 존재함
④ -OTs기는 좋은 이탈기이므로 좌측이 더 SN2 치환반응을 잘 함
⑤ 알킬기는 활성 증가 치환기이고 -Br기는 활성 감소 치환기임
4. 각 반응에서 최종 주생성물 A와 B의 구조로 옳게 짝지어진 것은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
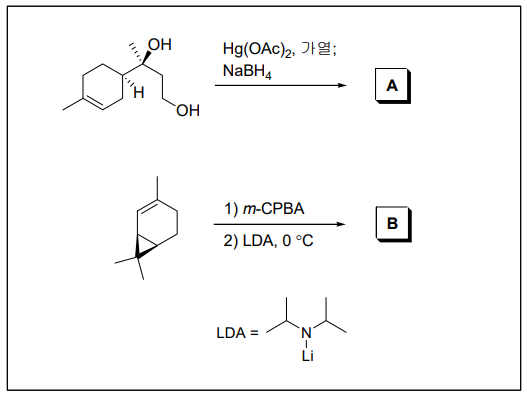
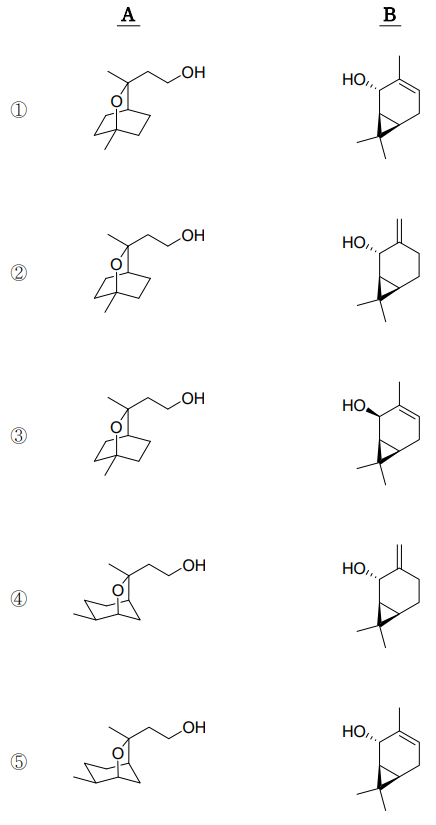
⑵ 풀이 : ②
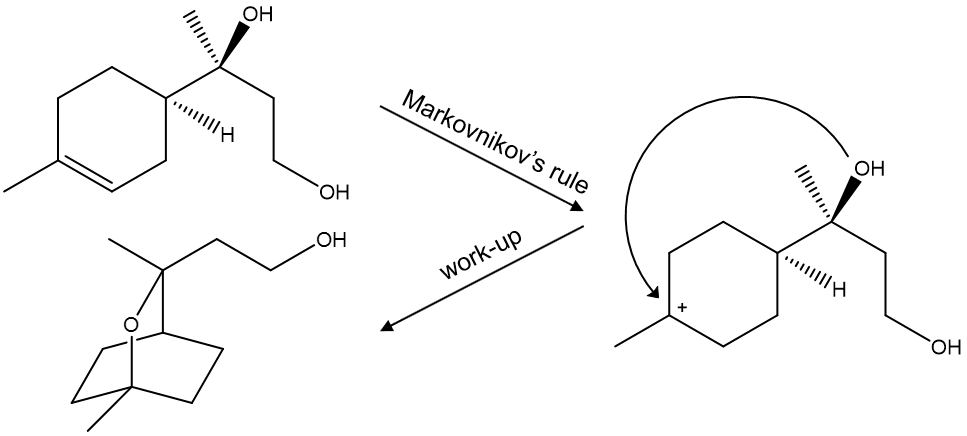
○ 첫 번째 반응 : 옥시수은화-탈수은화 반응 결과 알켄이 mercury-bridged carbocation 중간체가 됨. 다음 반응식은 이를 간단하게 carbocation으로 나타낸 것이고, 일반적인 수화반응이 아니라 분자 내 SN2 반응으로 종결시킴. 다치환 탄소양이온은 안정하므로 반응식과 같은 탄소양이온 선택성이 나타남
○ 두 번째 반응 : LDA는 Hofmann E2 elimination reaction을 일으키므로,
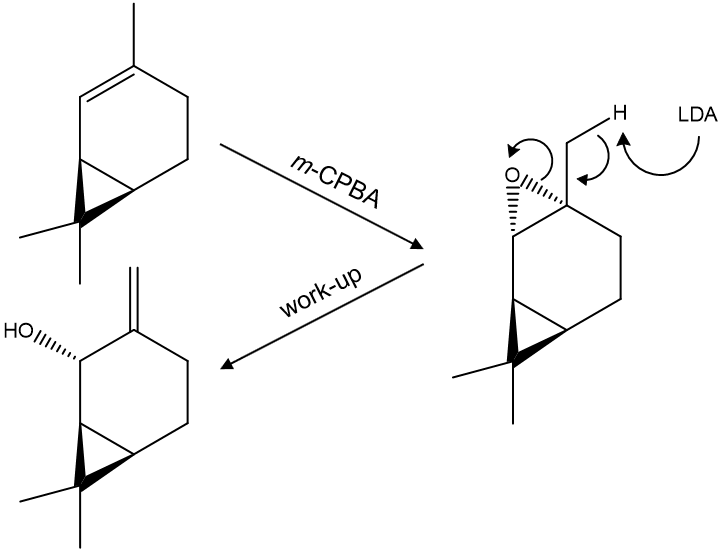
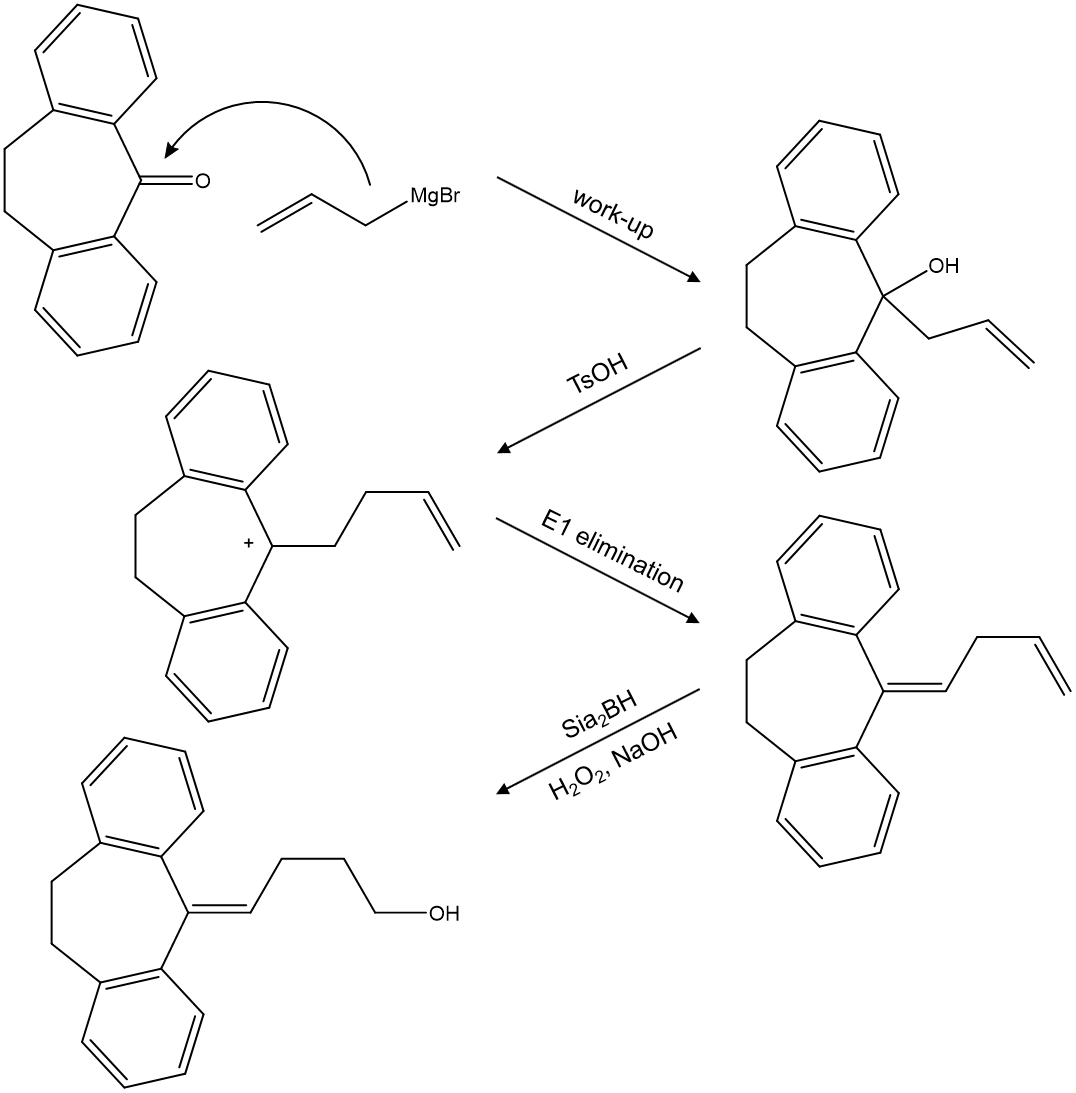
5. 다음 합성 과정에서 주생성물 A와 B의 구조로 옳게 짝지어진 것은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
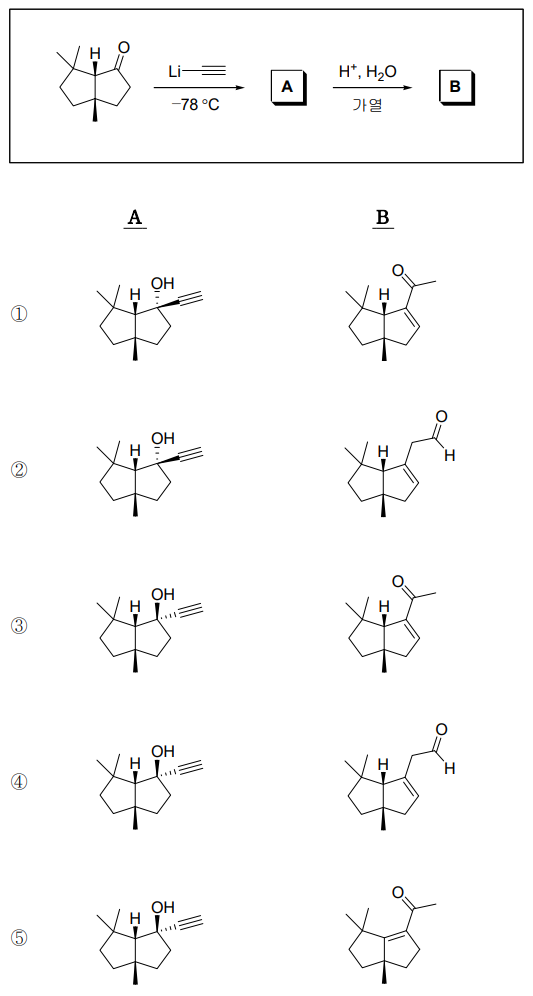
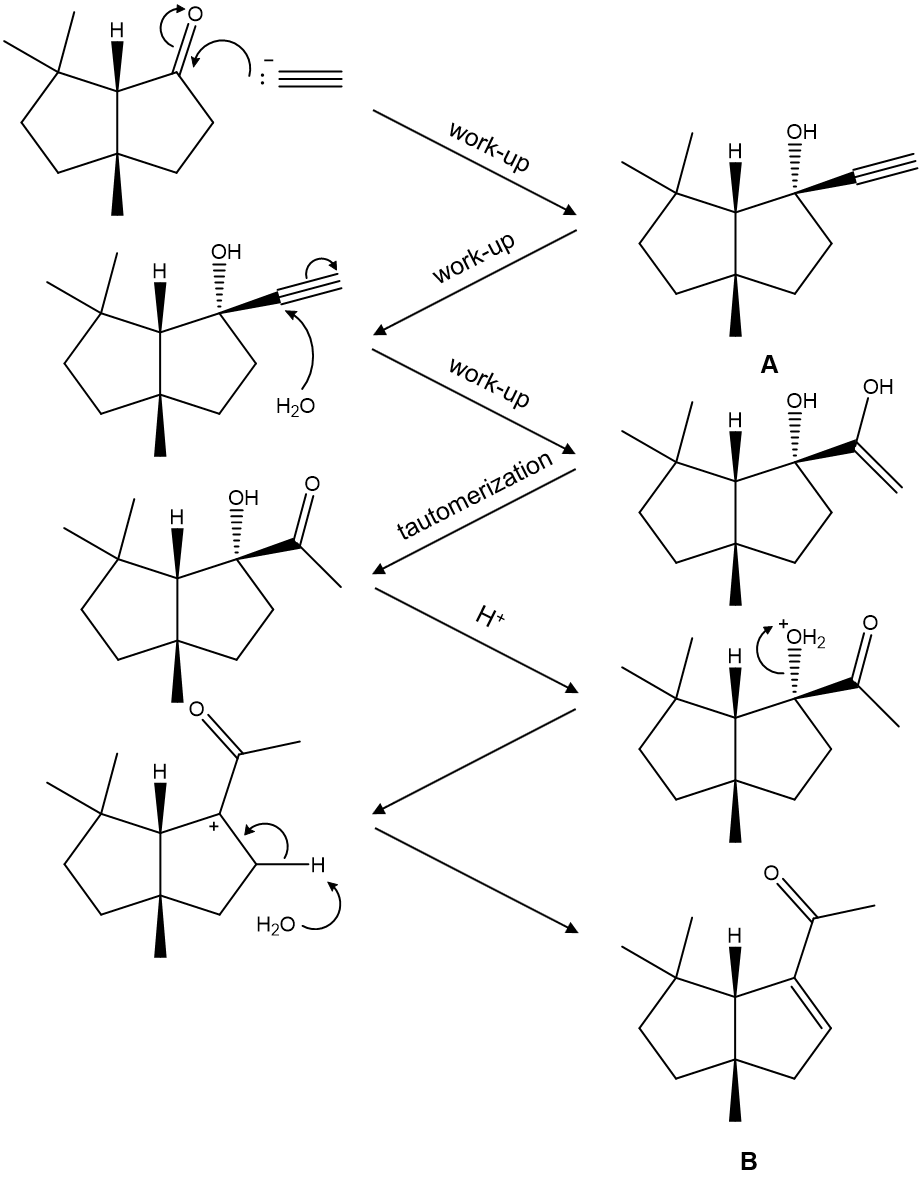
⑵ 풀이 : ①
○ 첫 번째 반응 : 평면 위에서 접근하는 게 평면 아래에서 접근하는 것보다 전자 반발이 덜하므로,
○ 두 번째 반응 : alkyne hydration reaction + E1 elimination reaction (구조 변화를 수반하지 않도록 수소가 제거돼야 함)
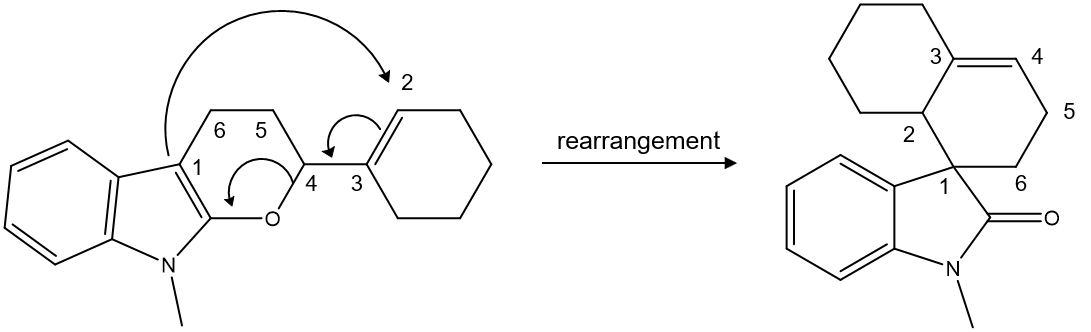
6. 〈예시〉는 클라이젠 재배열(Claisen rearrangement)을 나타낸 것이다. 화합물 A로부터 클라이젠 재배열이 일어난 반응의 주생성물 B의 구조로 옳은 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
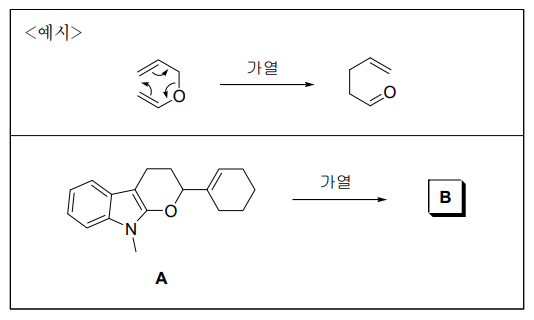
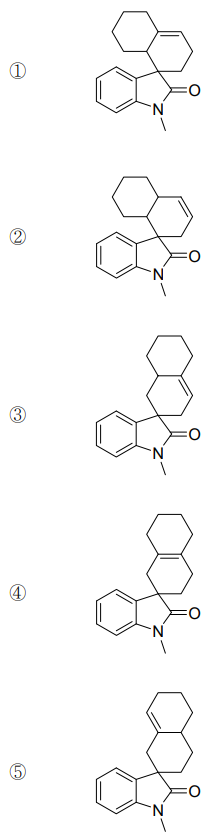
⑵ 풀이 : ①
7. 각 반응에서 최종 주생성물 A와 B의 구조로 옳게 짝지어진 것은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
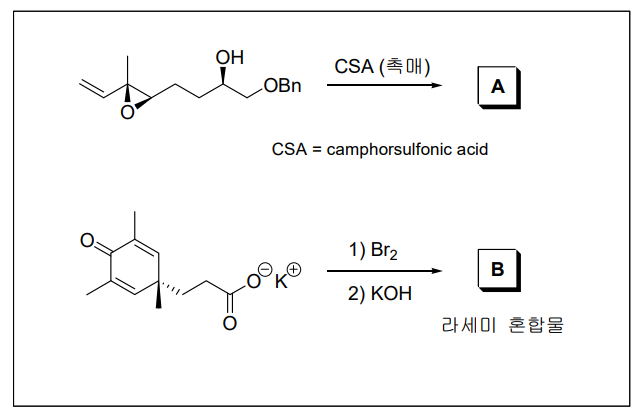
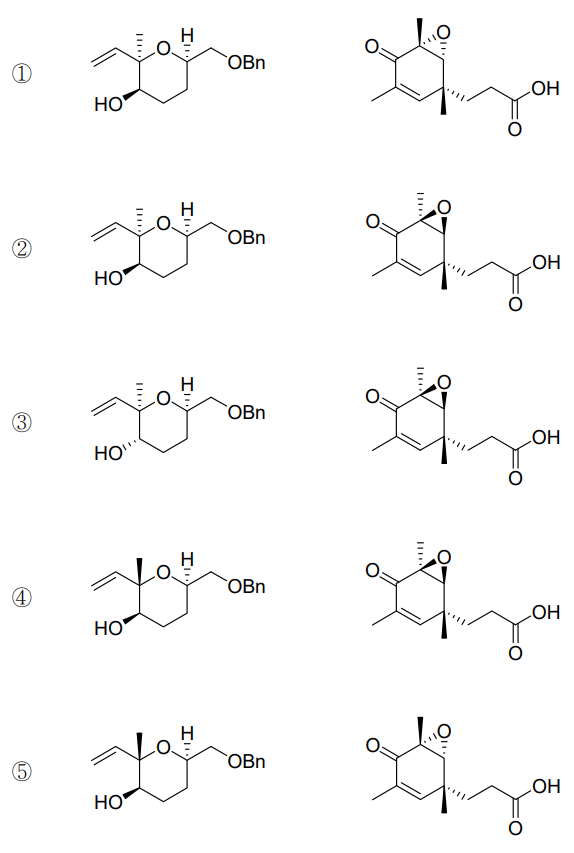
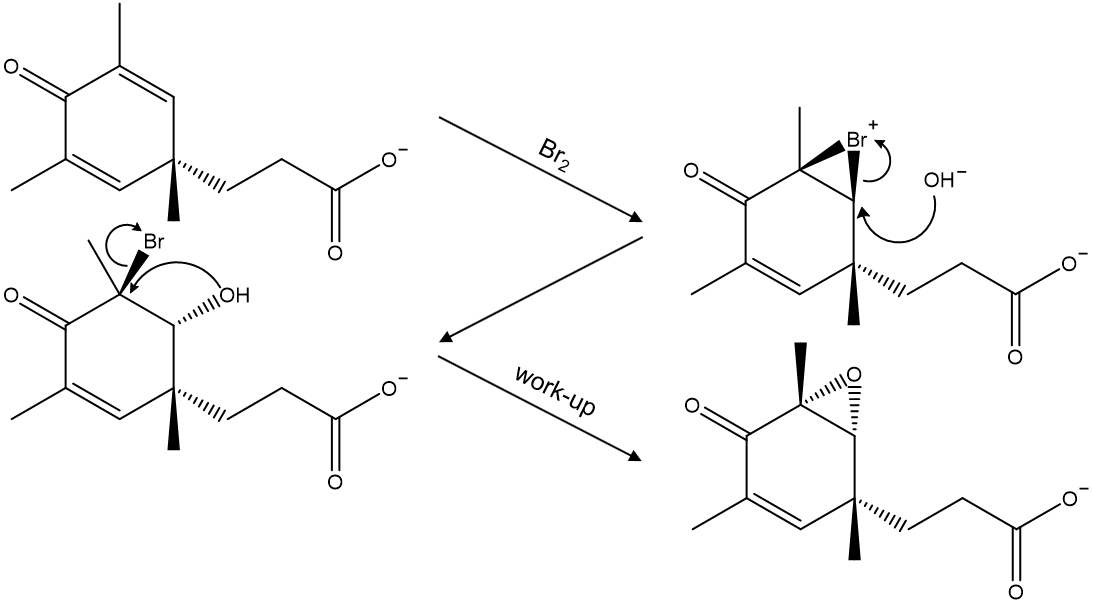
⑵ 풀이 : ⑤
○ 첫 번째 반응 : acid-catalyzed epoxide ring-opening reaction
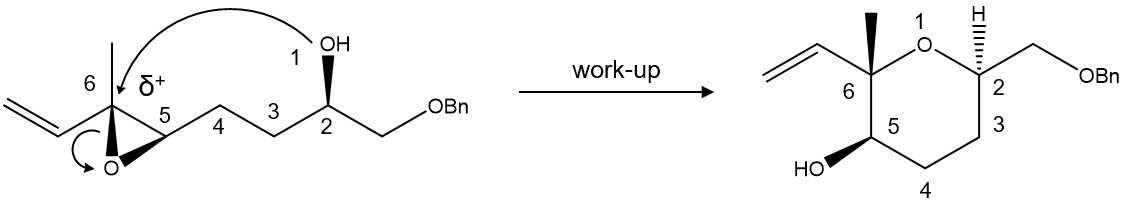
○ 두 번째 풀이
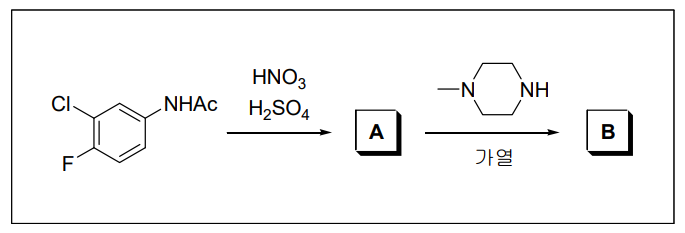
8. 다음 합성 과정에서 주생성물 A와 B의 구조로 옳게 짝지어진 것은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
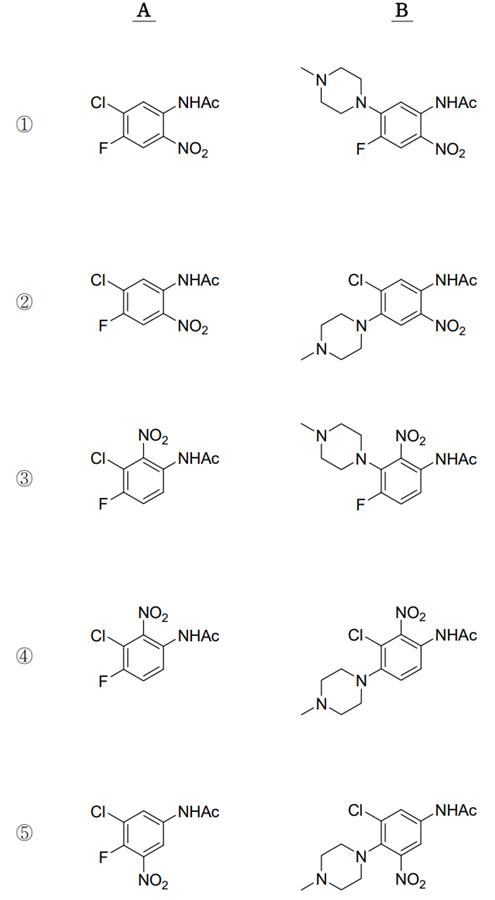
⑵ 풀이 : ①
○ 첫 번째 반응 (EAS)
○ -NHAc는 -Cl, -F보다 훨씬 강한 EDG이므로 -NHAc의 ortho 또는 para 배향이어야 함
○ 입체장애를 고려하면 -NHAc의 ortho 배향 중 ①의 좌측 형태와 같은 배향이 타당함
○ 두 번째 반응 (SNAr)
○ 첨가 후 제거 반응
○ EWG인 -NO2기가 안정화할 수 있는 공명유도체를 가지도록 F가 아니라 Cl에 첨가되는 게 타당함
9. 다음 각 반응의 주생성물 구조로 가장 적절한 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
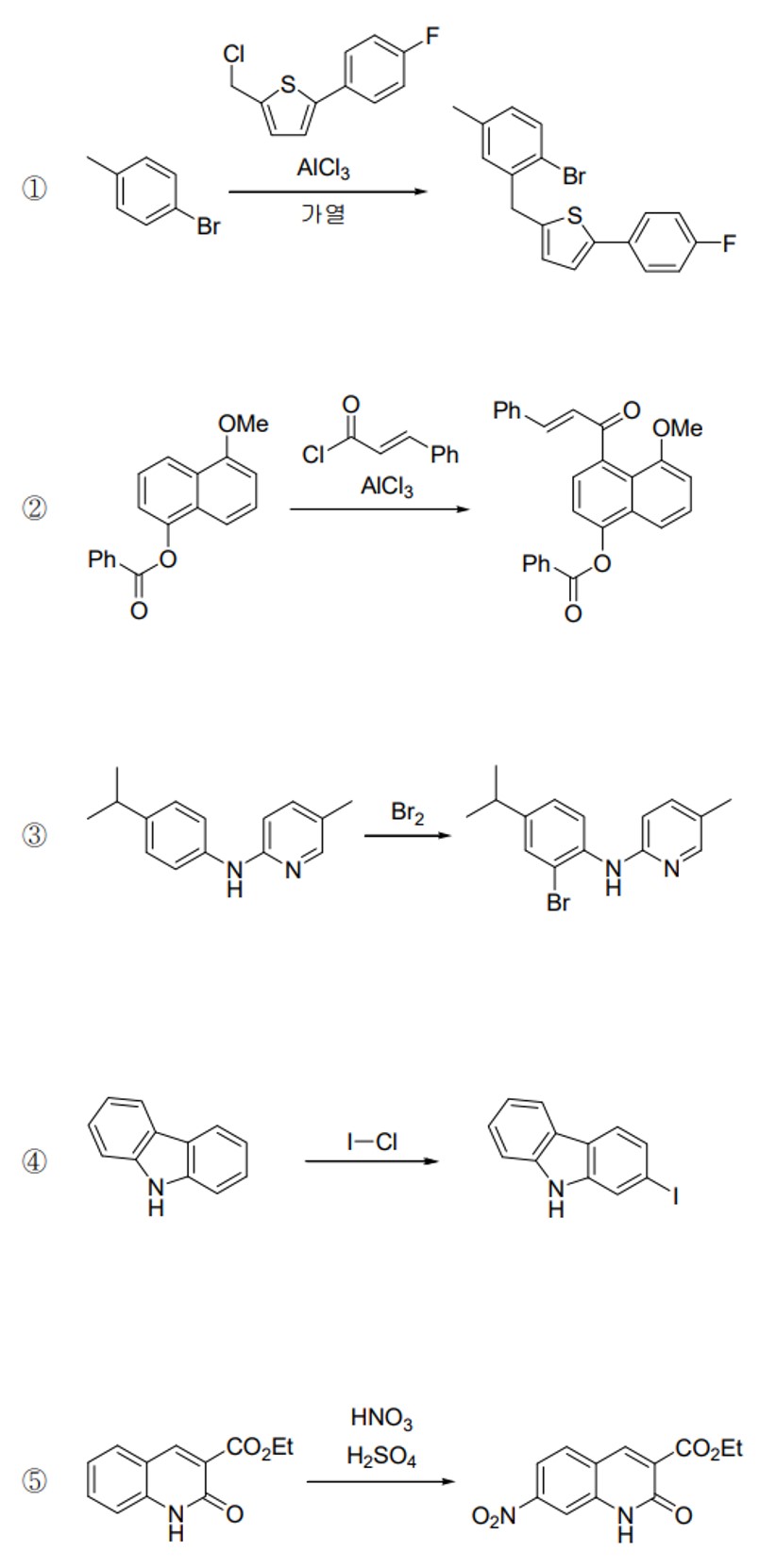
⑵ 풀이 : ③
① 주생성물 구조
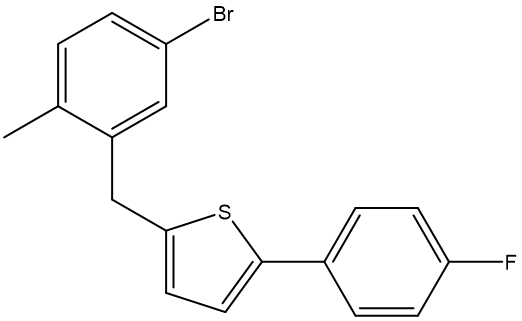
○ 원칙 : 할로젠기와 메틸기가 경합하는 경우 할로젠기의 ortho 배향으로 방향족 친전자성 반응이 일어남
○ 주어진 primary alkyl halide의 경우 AlCl4가 분리돼 나오지 않고 약하게 C-Cl 결합이 살아 있음
○ 그 결과 방향족 고리의 친전자성 반응의 경우 입체장애를 고려해야 하므로 위와 같이 methyl기의 ortho 배향이 타당
② 주생성물 구조
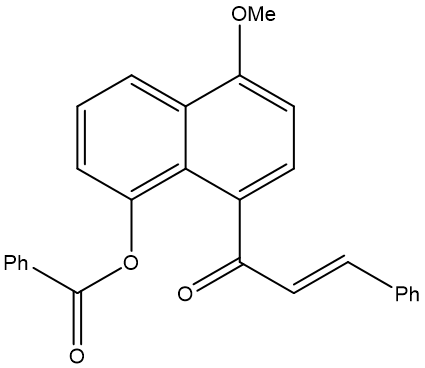
○ -OMe기는 활성 증가 치환기이고 EDG임
○ -CO2Ph기는 활성 감소 치환기이고 EWG임
○ -OMe기가 붙은 방향족 고리에서 -OMe기로부터 홀수 번, -CO2Ph기로부터 짝수 번 떨어진 지점에 치환이 이루어짐
○ -OMe기의 ortho 배향 및 para 배향이 가능할 수 있는데 para 배향인 게 입체장애 관점에서 유리함
③ 주생성물 구조 : 주어진 결과와 같음
○ benzene 고리가 pyridine 고리에 비해 orbital 겹침이 좋아 EAS 반응이 유리함 → 왼쪽 고리에 치환이 일어남
○ 아민기가 R기보다 강한 EDG이므로 아민기의 ortho, para 배향이 되도록 함
④ 주생성물 구조
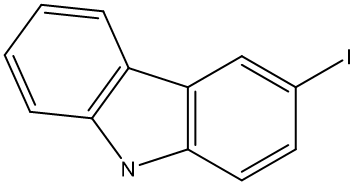
○ 아민기가 R기보다 강한 EDG이므로 아민기의 ortho, para 배향이 되도록 함
⑤ 주생성물 구조
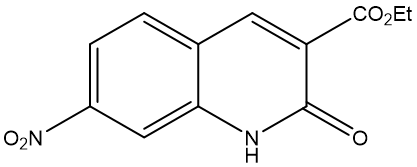
○ 강한 EDG인 아민기로부터 홀수 번, 강한 EWG인 -CO2Et기로부터 짝수 번 떨어진 지점에서 치환이 이루어짐
○ 두 위치가 경합하므로 입체장애를 고려해야 함
10. 출발 물질 A로부터 다단계 반응을 거쳐 최종 주생성물 B를 합성하려고 할 때, 가장 적절한 반응 과정은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
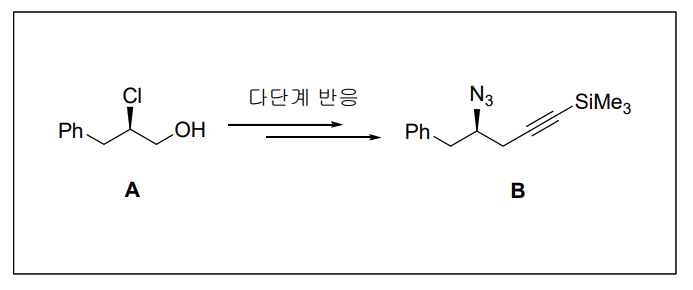
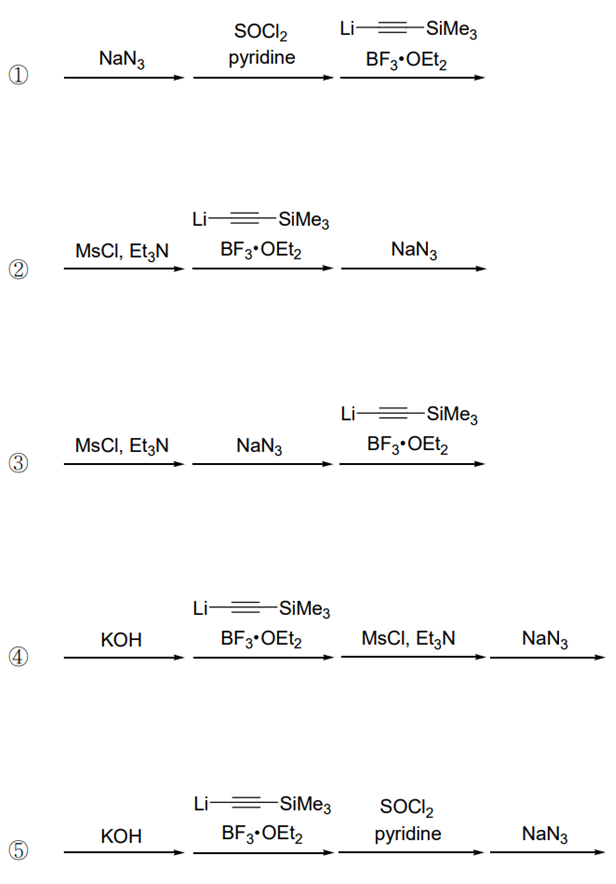
⑵ 풀이 : ④
① alkyl halide SN2 substisution → alcohol SN2 substitution → RLi coupling reaction
○ -N3기의 배향이 적절하지 않음
② alcohol mesylation → RLi coupling reaction → alkyl halide SN2 substitution reaction
○ -N3기의 배향이 적절하지 않음
③ alcohol mesylation → alkyl halide SN2 substitution → RLi coupling reaction
○ -N3기가 다른 위치에 생성됨
④ alkyl halide SN2 substitution → RLi coupling reaction → alcohol mesylation → SN2 substitution
⑤ alkyl halide SN2 substitution → RLi coupling reaction → alcohol SN2 substitution → SN2 substitution
○ -N3기의 배향이 적절하지 않음
11. 다음은 출발 물질 A로부터 주생성물 B를 합성하는 〈반응식〉과 〈실험 과정〉이다. 이 실험에 대한 설명으로 가장 적절한 것은?
⑴ 문제
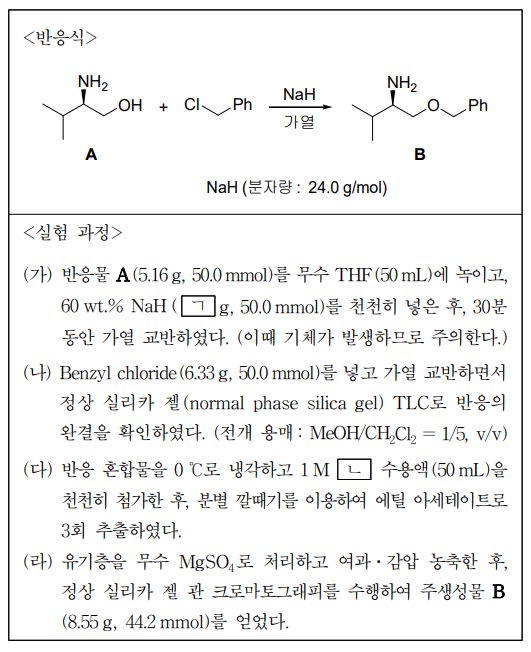

⑵ 풀이 : ④
① 무수 THF에서 Na2CO3의 용해도는 나쁨
② 60 wt.%를 고려하여 2.00이 돼야 함
③ 주로 발생하는 기체는 수소기체(H2)임
④ A가 B보다 극성이 강하므로 전개도가 떨어짐
⑤ NaOH 수용액을 사용하여 A와 B를 분리해야 함
12. 주어진 이름의 출발 물질로부터 각 반응을 통하여 얻어지는 주생성물의 구조가 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
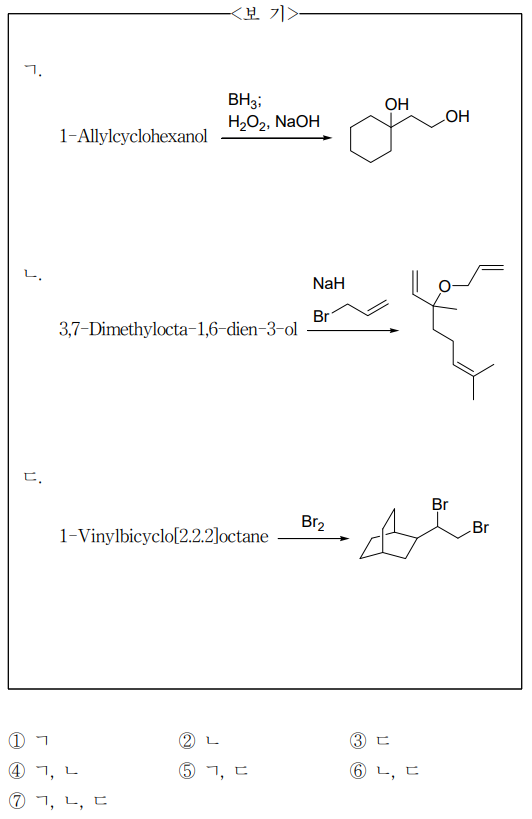
⑵ 풀이 : ②
○ ㄱ. hydroboration-oxidation reaction. 생성물의 탄소의 개수가 부족함
○ ㄴ. -OH기를 NaH로 -O-로 만든 뒤 alkyl halide SN2 substitution reaction을 진행
○ ㄷ. bicycloalkane은 다리목 탄소를 1번으로 함
13. 두 화합물이 서로 거울상이성질체(enantiomer) 관계인 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제
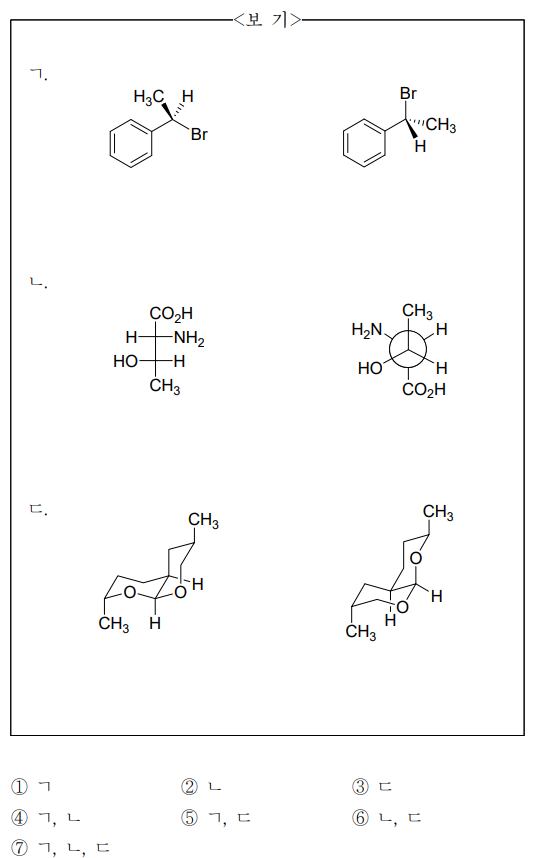
⑵ 풀이 : ②
○ ㄱ. 동일한 화합물 : 왼쪽과 오른쪽 모두 R
○ ㄴ. 거울상이성질체 : 왼쪽은 (2R, 3S), 오른쪽은 (2S, 3R) (참고로, -COOH기가 가장 우선순위가 높은 작용기)
○ ㄷ. 부분입체이성질체 : 왼쪽 구조의 왼쪽 아래 methyl기가 오른쪽 구조의 오른쪽 위 methyl기와 대응됨을 유의할 것
14. 각 반응에서 주생성물 내에 존재하는 카이랄 중심의 절대 배열이 R인 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
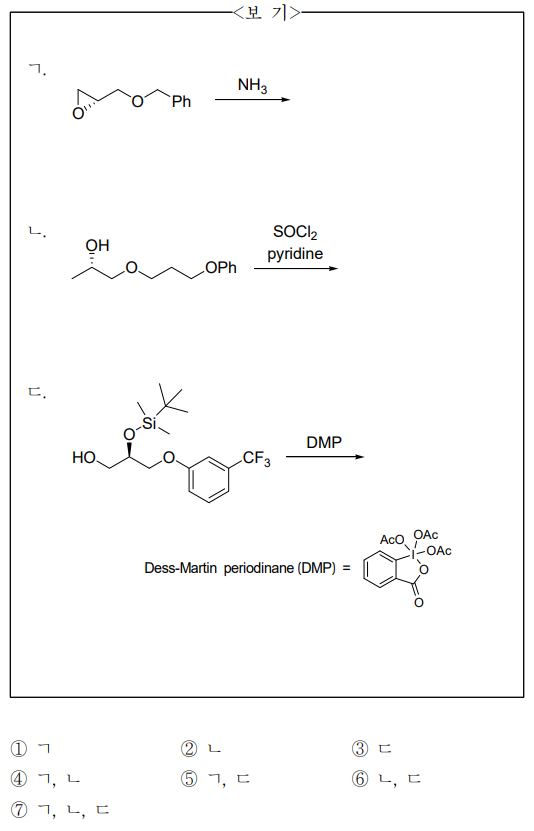
⑵ 풀이 : ④
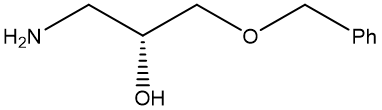
○ ㄱ. base-catalyzed epoxide ring-opening reaction
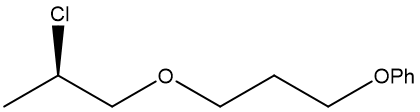
○ ㄴ. alcohol SN2 substitution reaction
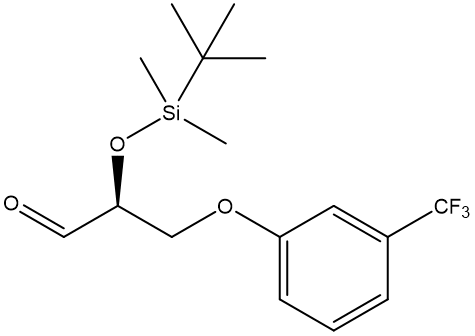
○ ㄷ. Dess-Martin oxidation
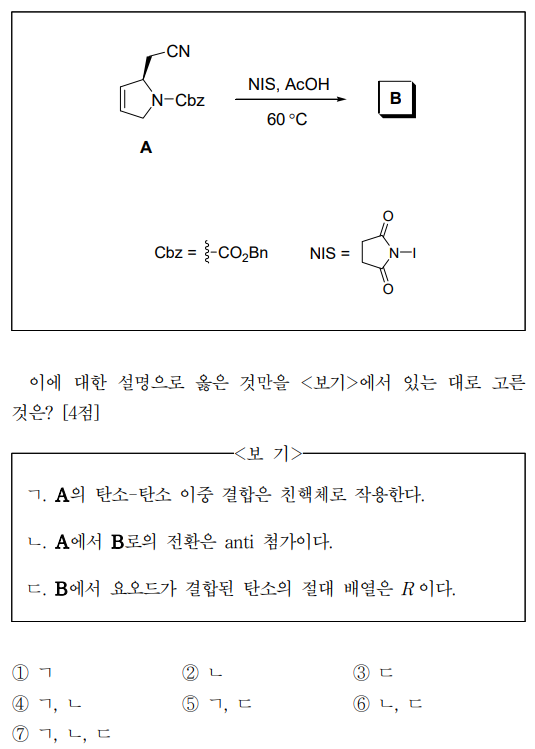
15. 다음은 출발 물질 A로부터 주생성물 B를 합성하는 반응이다. (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.) 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제
⑵ 풀이 : ⑦
○ ㄱ. 알켄은 전자가 풍부하므로 전자를 제공하는 친핵체로 작용
○ ㄴ. alkene electrophilic addition with NIS and acetic acid
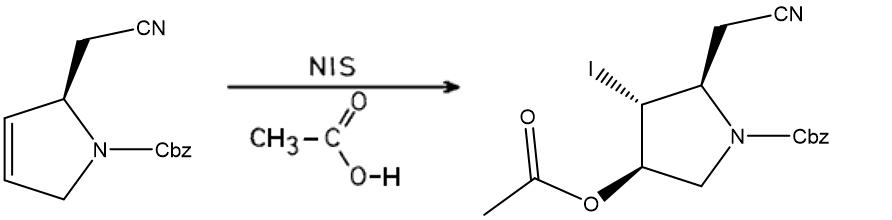
○ ㄷ. R임
16. 주생성물의 구조가 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
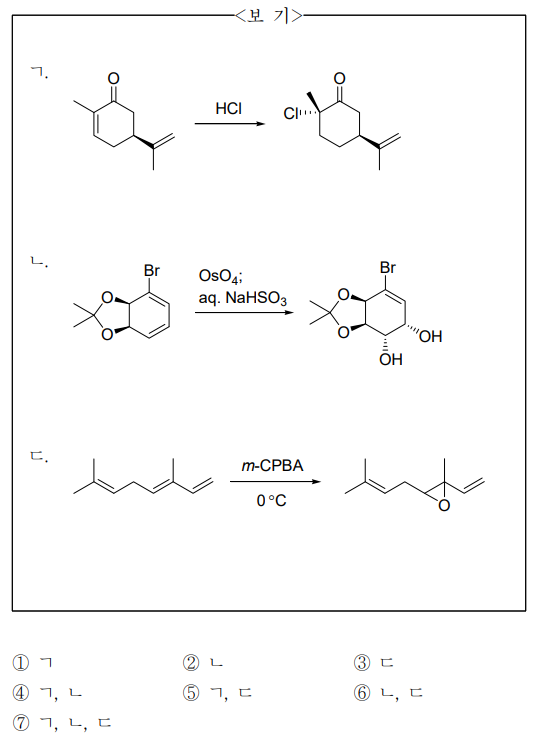
⑵ 풀이 : ②
○ ㄱ. -C=O기는 EWG이므로 탄소양이온은 아래쪽에 생겨야 함
○ ㄴ. 입체장애가 적은 알켄에 syn-diol을 형성함
○ ㄷ. m-CPBA는 다치환 알켄을 선호하며, conjugated diene의 경우 완전한 C=C 이중결합이라 할 수 없어 반응성이 낮음
17. 최종 주생성물의 구조가 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
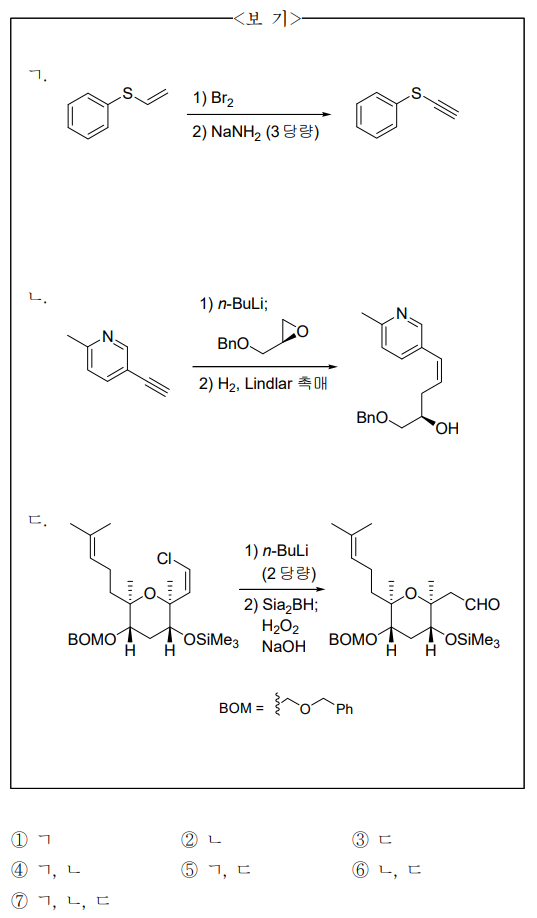
⑵ 풀이 : ⑦
○ ㄱ. alkene halogenation → E2 elimination (excess)
○ ㄴ. n-BuLi as base → base-catalyzed epoxide ring-opening reaction (less steric) → alkyne Lindlar catalytic reaction
○ ㄷ. n-BuLi as base → alkene to alkyne → hydroboration-oxidation reaction → tautomerization
18. 주생성물의 구조가 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
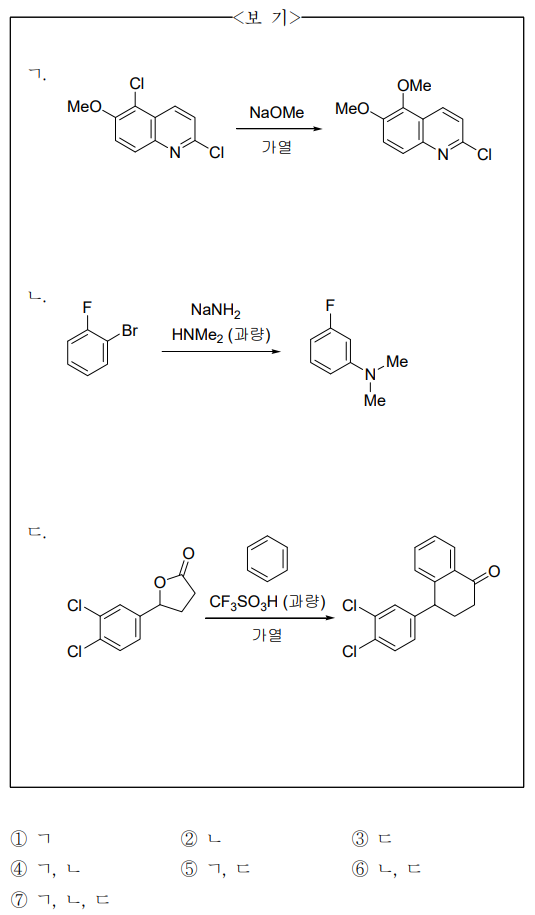
⑵ 풀이 : ⑥
① 친핵성 방향족 첨가반응(SNAr)에서 음전하 중간체를 안정화할 수 있도록 pyridine 고리에 첨가돼야 함
② 친핵성 방향족 첨가반응 중 제거 후 첨가반응
○ -F는 일반적으로 EDG이지만, 벤자인에 있어서 -F기의 공명 효과가 없으므로 EWG로 고려함
○ F가 붙은 탄소의 ortho 배향의 탄소보다 meta 배향의 탄소의 음하전이 강함
○ 그러므로 F가 붙은 탄소의 meta 배향으로 아민기가 결합함
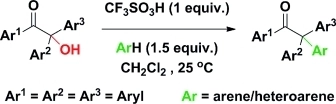
③ CF3SO3H Friedel-Crafts arylation은 -OH기를 제거하고 방향족 고리를 붙임
Figure. 1. CF3SO3H Friedel-Crafts arylation
19. 주생성물의 구조가 옳은 것만을 〈보기〉에서 있는 대로 고른 것은? (단, 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.)
⑴ 문제
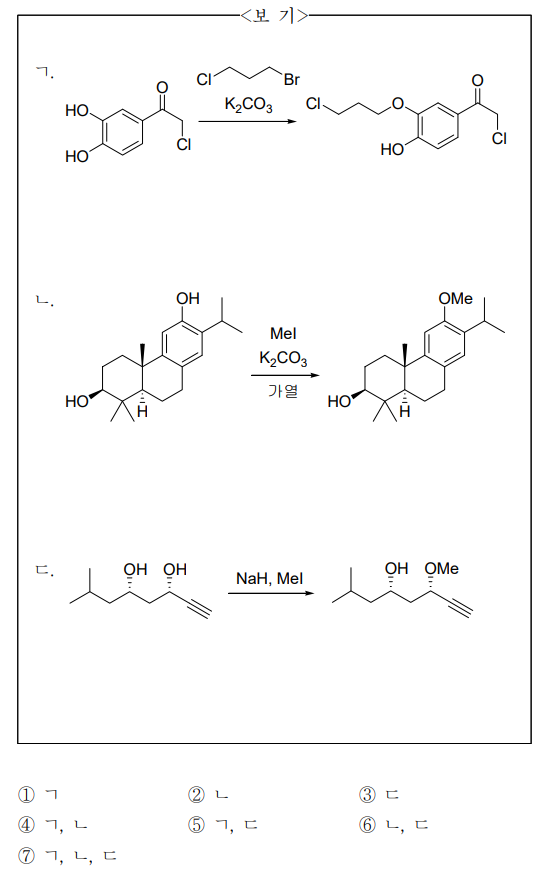
⑵ 풀이 : ⑥
○ ㄱ. 분자 내 SN2 반응을 고려해야 함
○ ㄴ. K2CO3 as base → alkyl halide SN2 substitution reaction
○ ㄷ. -OH기가 alkyne보다 산도가 강하고, sp 탄소가 sp3 탄소보다 전기음성도가 강함
20. 다음은 출발 물질 A로부터 주생성물 B와 C를 거쳐 주생성물 D를 합성하는 〈반응식〉과 과정 (가)에 관련된 〈시약〉이다. (단, 각 단계에서 주생성물은 적절한 분리·정제 과정을 통하여 얻는다.) 이에 대한 설명으로 옳은 것만을 〈보기〉에서 있는 대로 고른 것은?
⑴ 문제
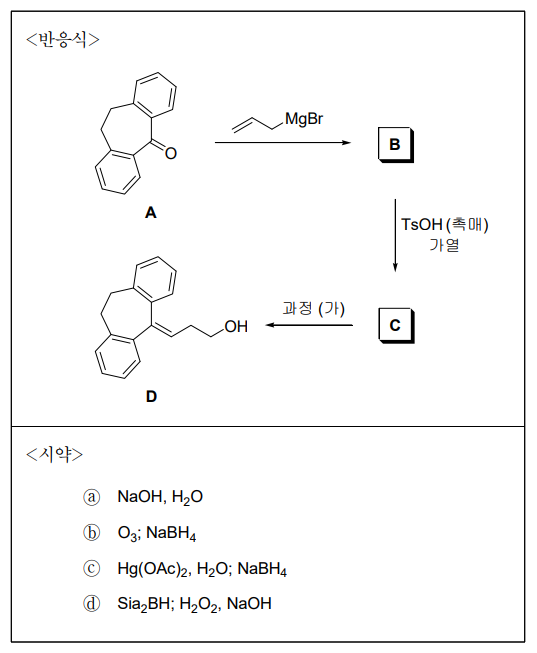

⑵ 풀이 : ⑤
입력: 2021.07.15 13:50
'▶ 자연과학 > ▷ MEET∙DEET∙PEET 풀이' 카테고리의 다른 글
| 【유기화학】 2019 PEET 유기화학 (11) | 2021.07.26 |
|---|---|
| 【유기화학】 2020 PEET 유기화학 (4) | 2021.07.23 |
| 【화학】 2017 MEET/DEET 화학 (예비검사) (0) | 2021.02.05 |
| 【유기화학】 2021 MEET/DEET 유기화학 (10) | 2020.08.26 |
| 【화학】 2016 MEET/DEET 화학 (6) | 2020.06.30 |




최근댓글