추천글 : 【유기화학】 변리사 2차 유기화학 풀이
유기초심자 님 지적사항 수정 (23.07.01)
문제 1. 화합물 A를 vinyl Grignard 시약(CH2CHMgBr)과 반응시켰더니 C10H14O의 같은 조성을 갖는 두 개의 화합물 B와 C의 혼합물이 생성되었다. 두 개의 화합물 중에서 화합물 B는 320 ℃로 가열하였더니 Cope rearrangement 반응을 하여 중간체 D를 거쳐 C10H14O의 조성을 갖는 최종 생성물 E가 되었으나, 화합물 C는 같은 조건에서 Cope rearrangement 반응을 하지 않았다.

⑴ 반응 메커니즘

⑵ 화합물 B와 C의 Cope rearrangement 반응에 대한 반응성의 차이를 반응 메커니즘을 고려하여 설명하시오.
○ Cope rearrangement처럼 기존 결합이 끊어지고 새로운 결합이 생성될 때 유사 콘쥬게이션 중간체를 거침
○ 즉, C의 경우 자리이동반응을 위한 오비탈 겹침이 어렵기 때문에 반응성이 떨어짐
○ 만약 유사 콘쥬게이션 중간체를 거치지 않으면 반응 활성화에너지가 높아져서 반응이 진행되지 않음
문제 2. 다음 두 반응에 대한 물음에 답하시오.
⑴ 문제 2-1. o-chlorotoluene은 KNH2와의 반응에서 두 개의 생성물 A와 B로 변환된다. A와 B의 구조를 밝혀라.

⑵ 답 2-1. 제거 후 첨가 반응
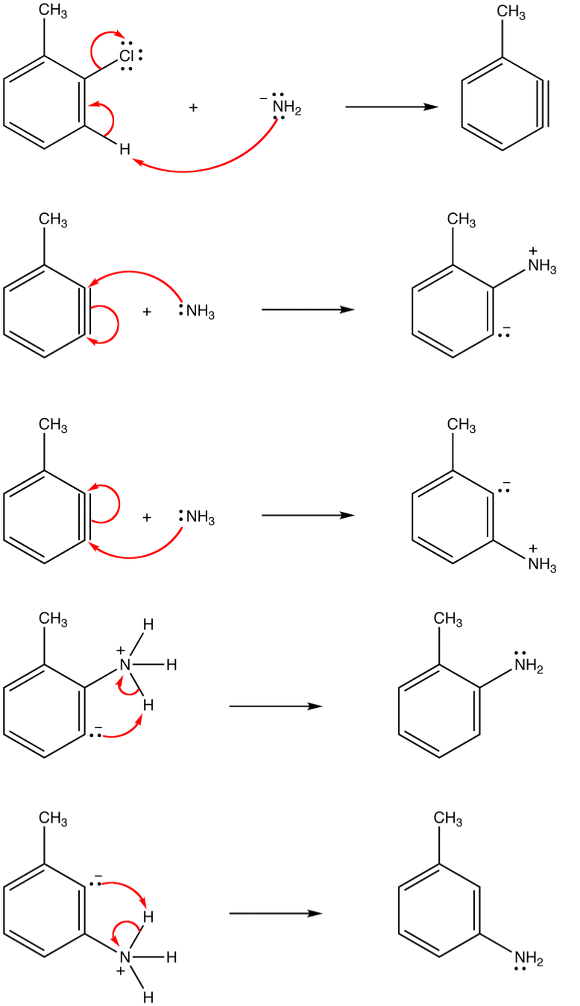
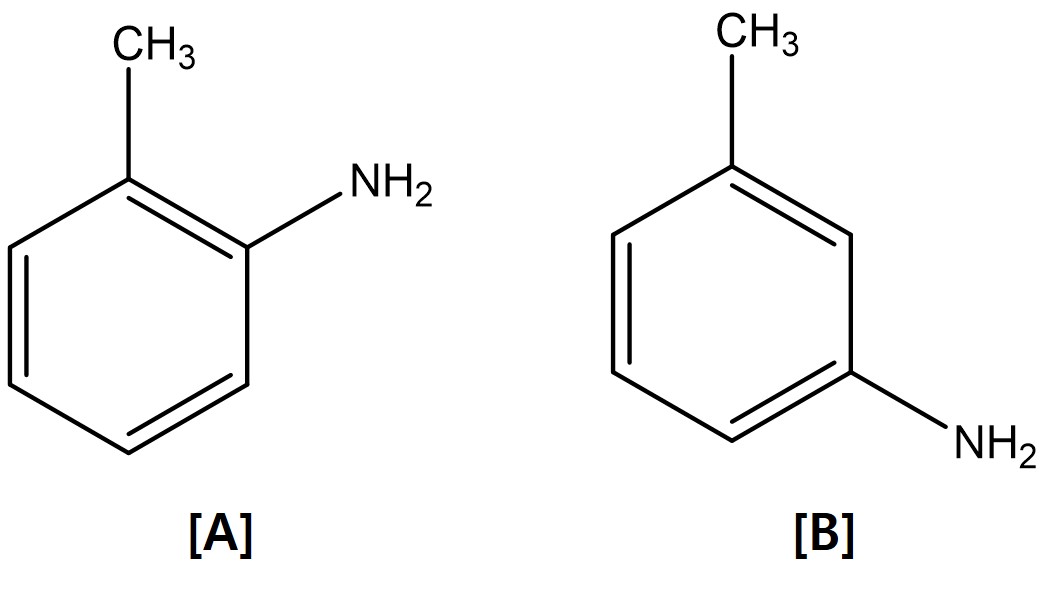
⑶ 문제 2-2. 1H-indene은 다음 반응조건에서 C10H8Cl2의 조성을 갖는 중간체 A를 거쳐 C10H7Cl의 조성을 갖는 최종생성물 B로 변환한다. A와 B의 구조를 밝혀라.

⑷ 답 2-2.
① 반응 메커니즘
○ carbene formation reaction → ring opening reaction
○ 반응식을 보고 불포화도를 계산하여 다중결합 및 고리의 총합의 수를 가늠해 볼 수 있음
② 정답 풀이
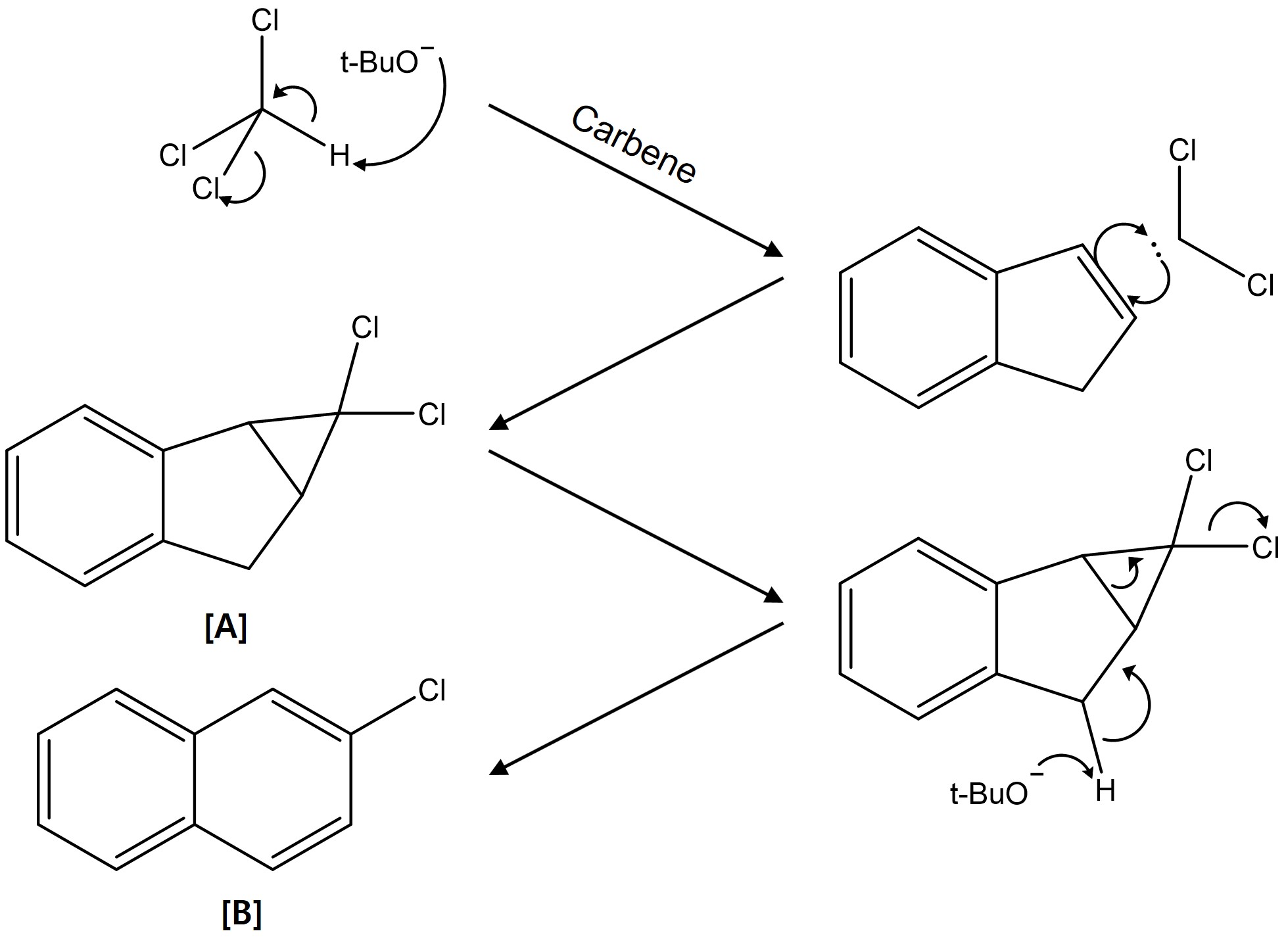
○ 특징 : 방향족성에 의해 반응이 선호됨
③ 오답 유형
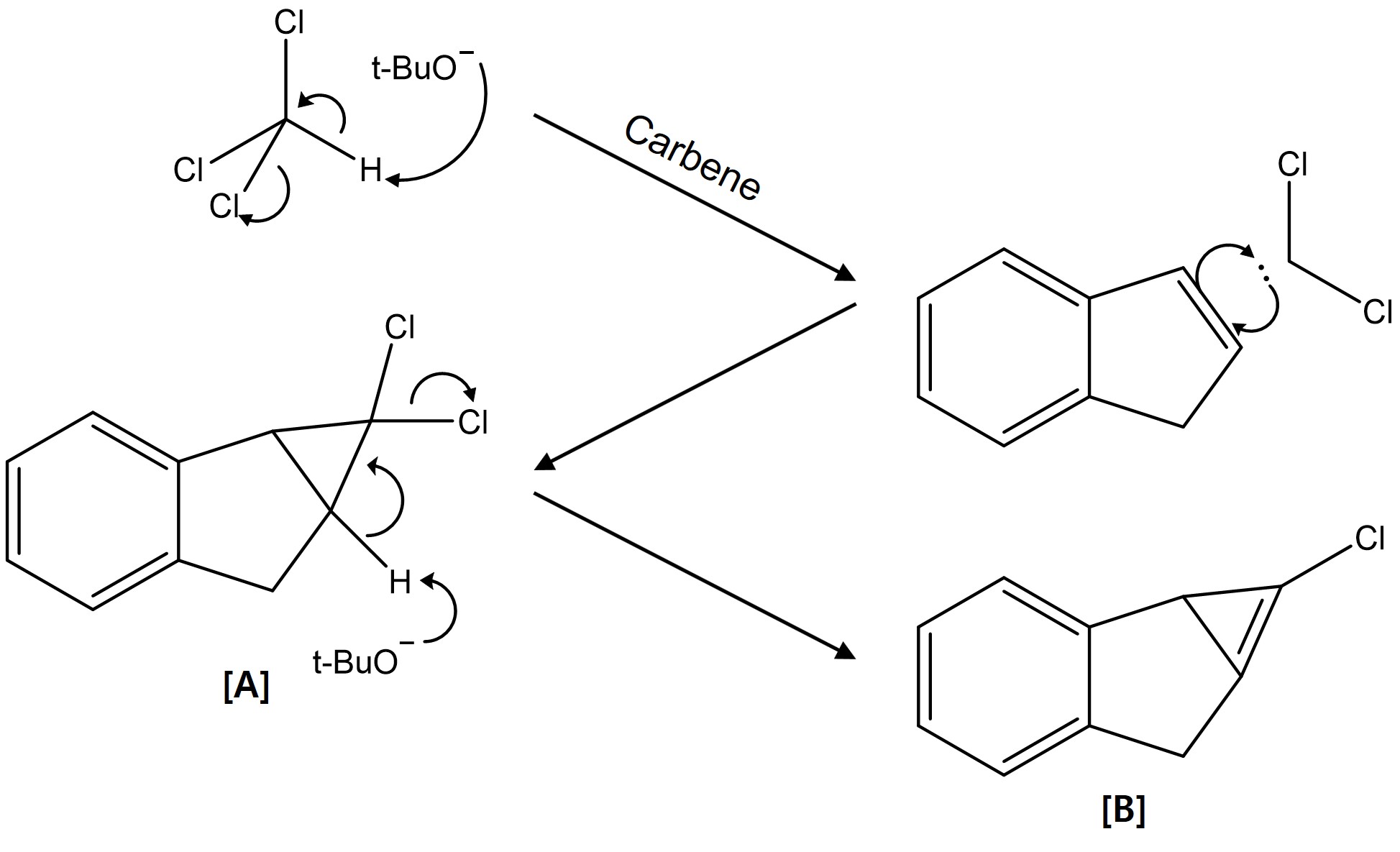
○ 특징 : 삼각고리 내 이중결합이 있는 경우 ring strain이 너무 큼
문제 3. 다음은 t-부탄올 (t-butanol)(A)의 황산(H2SO4) 촉매에 의한 2-메틸프로펜(2-methylpropene)(B)로의 탈수반응이다. 이 반응의 역반응은 수화반응은 t-부탄올 제법으로 이용될 수 있다.

⑴ 문제 3-1. 정반향의 탈수 반응에서 속도결정단계를 지정하라.
⑵ 답 3-1. E1 제거반응이다. -OH2+가 해리되어 탄소양이온이 생성되는 단계가 속도결정단계이다. 반응속도는 반응물에 1차적으로 비례하기 때문에 제거(elimination)의 E와 1차의 1이 반응명을 구성하게 됐다.
⑶ 문제 3-2. 반응물 A로부터 생성물 B와 H2O 분자로 전환되는 탈수반응에서 끊어지고 만들어지는 결합들의 결합세기를 토대로 반응 엔탈피 변화(ΔHº)의 부호를 예측하고, 이 반응이 발열반응인지 흡열반응인지 밝히시오. 그리고 문제 3-1의 정방향 탈수반응에서의 반응 엔트로피 변화(ΔSº)를 예측하고 그 부호를 밝히시오.
⑷ 답 3-2. 안정한 σ 결합 한 개가 깨지고 불안정한 π 결합 한 개가 생겼다. A → B가 되면서 불안정해졌으므로 ΔH > 0이다. 반면 생성물의 수가 반응물의 수보다 많으므로 ΔSº > 0이다.
⑸ 문제 3-3. 가역 평형반응에서 평형상수를 결정하는 자유에너지 변화 (ΔGº)와 반응 엔탈피 변화 (ΔHº), 그리고 엔트로피 변화 (ΔSº) 사이의 관계식을 쓰고, 또한 자유에너지 변화( ΔGº)와 평형상수 (K)와의 관계식을 쓰시오.
⑹ 답 3-3.
① ΔGº = ΔHº - TΔSº
② ΔGº = -RT lnK
⑺ 문제 3-4. 문제 3-3에서 구한 관계식을 이용하여 정방향 탈수반응의 생성물 농도를 증가시키기 위한 온도조절에 대해 기술하시오.
⑻ 답 3-4. ΔGº < 0이 되기 위해서는 TΔSº (>0) 항이 커져야 한다. 따라서 온도가 증가해야 정방향으로 많이 치우칠 수 있다.
문제 4. 다음은 유기합성에 중요하게 사용되는 Diels-Alder 반응에 대한 물음이다.
⑴ 문제 4-1. Diels-Alder 반응에서 아래 4가지 친다이엔체(dienophile)를 반응성이 큰 순서대로 나열하시오.

⑵ 답 4-1.
① Diels-Alder 반응에서, 다이엔(diene)은 전자가 많을수록 친다이엔체(dienophile)는 전자가 적을수록 반응성이 크다. ⒝ < ⒞ < ⒜ < ⒟ 순으로 반응이 빠르다.
② ⒝와 ⒞의 비교 : EWG가 없는 ⒝보다 EWG가 있는 ⒞가 더 반응성이 좋다.
③ ⒞와 ⒜의 비교
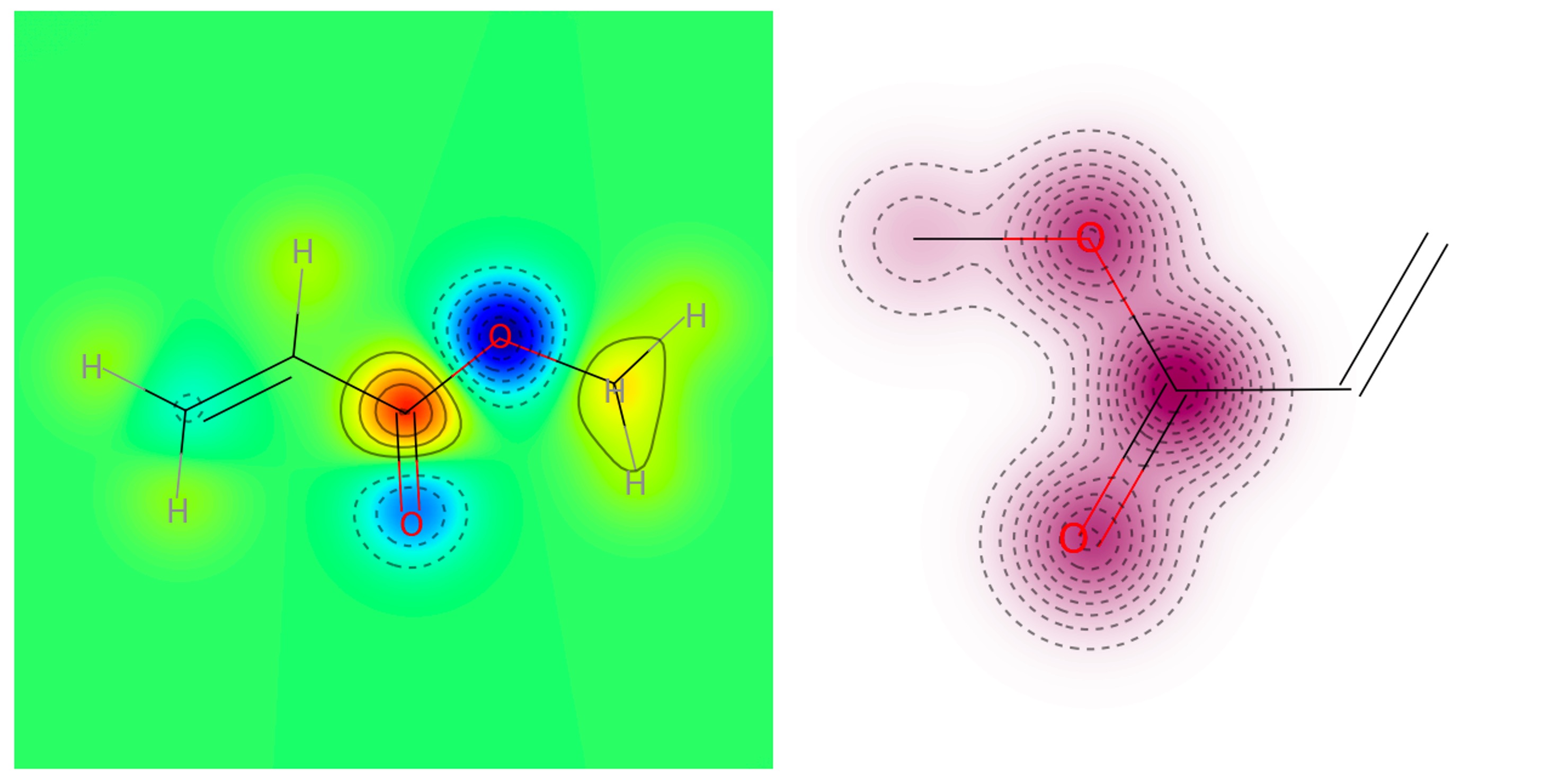
○ 일반적으로 -CO2Me기가 멀리 떨어져 있는 경우 -COMe보다 더 강력한 EWG로 작용한다. 그러나 이 문제는 다르다.
○ ⒜의 경우 알켄과 케톤이 쉽게 공명할 수 있다.
○ ⒞의 경우 에스터를 구성하는 sp2 탄소가 케톤 그룹과 메톡시 기 간의 공명을 통해 비교적 전자밀도가 높아진다. 이러한 차단효로 인해 알켄이 에스터와 쉽게 공명할 수 없어 친다이엔체의 반응성이 떨어진다.
④ ⒜와 ⒟의 비교 : EWG가 1개인 것보다 2개 이상인 경우 반응속도는 압도적으로 빨라진다.
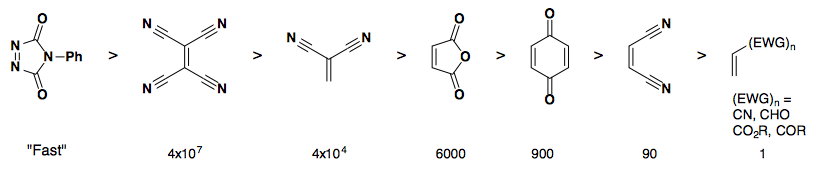
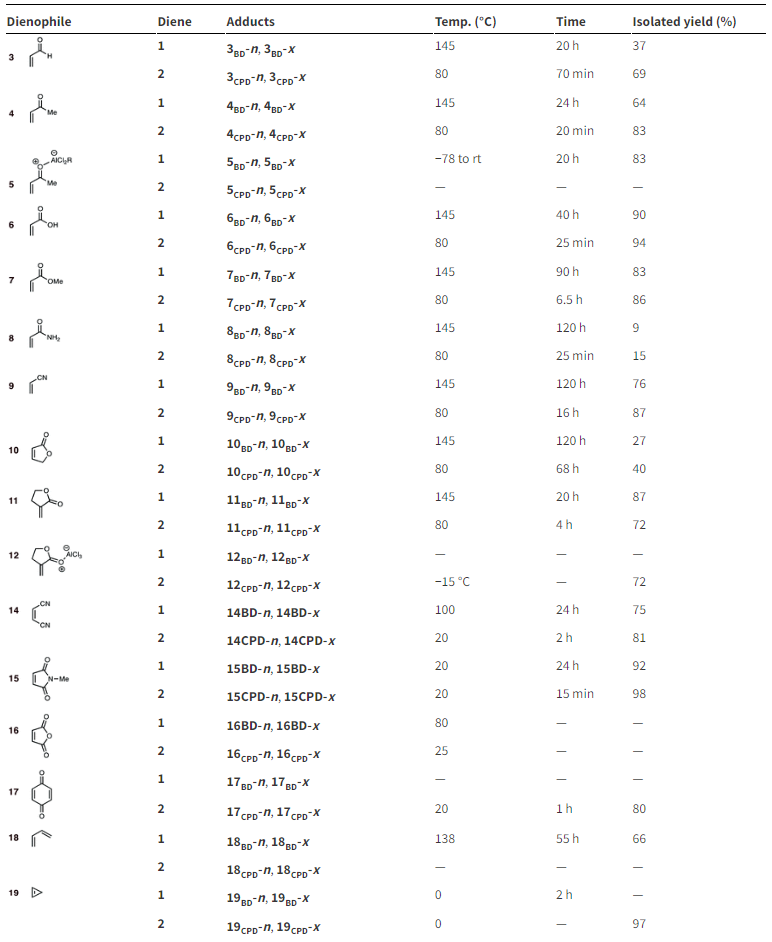
Table. 1. 친다이엔의 반응성 비교
⑶ 문제 4-2. 1,3-사이클로펜타다이엔(1,3-cyclopentadiene)과 에틸렌(CH2=CH2)의 반응에서 아래 두 가지 다른 조건에서 반응시킬 때에 두 반응물 사이에 생성되는 각각의 생성물 구조를 밝히시오.

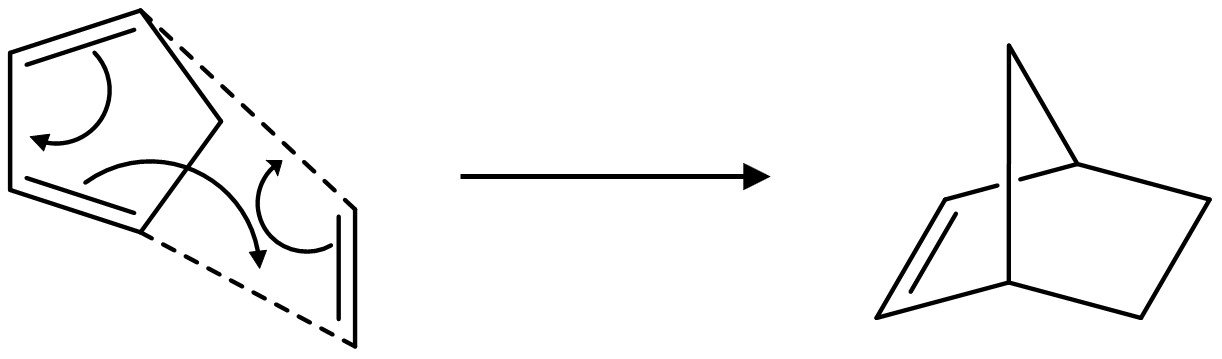
⑷ 답 4-2.
② hν 조건 : 2+2 고리화 반응
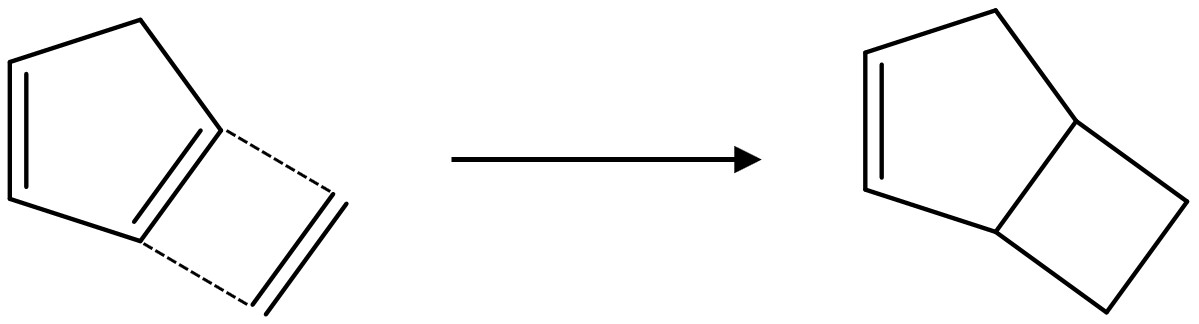
③ Δ 조건 : 4+2 고리화 반응
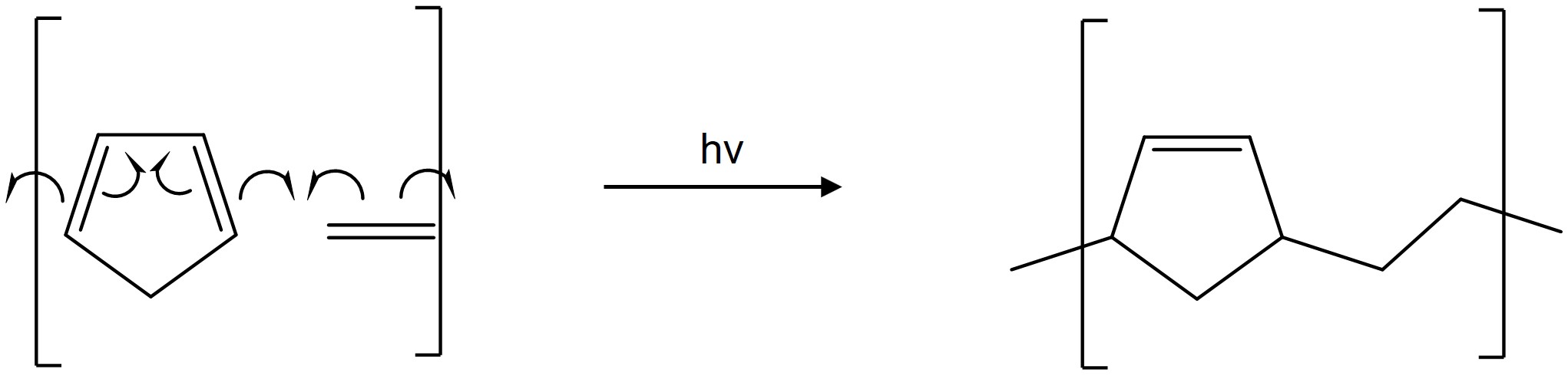
④ 참고로, hν 조건에서 중합 반응이 일어날 수 있음 (ref)
⑸ 문제 4-3. 1,3-부타다이엔(1,3-butadiene)과 다이에틸 말리에이트(diethyl maleate)와 그리고 다이에틸 푸마레이트(diethyl fumarate)를 각각 Diels-Alder 반응시킬 때 생성되는 생성물들을 표시하라.

⑹ 답 4-3.
① 첫 번째 : meso compound

② 두 번째 : racemic mixture

입력 : 2019.04.05 17:31
'▶ 자연과학 > ▷ 변리사 풀이' 카테고리의 다른 글
| 【유기화학】 2011년 제48회 변리사 2차 국가자격시험 (11) | 2019.04.05 |
|---|---|
| 【유기화학】 2012년 제49회 변리사 2차 국가자격시험 (5) | 2019.04.05 |
| 【유기화학】 2015년 제52회 변리사 2차 국가자격시험 (35) | 2019.04.05 |
| 【유기화학】 2016년 제53회 변리사 2차 국가자격시험 (6) | 2019.04.04 |
| 【유기화학】 2017년 제54회 변리사 2차 국가자격시험 (6) | 2019.04.04 |




최근댓글